

 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
 (2010?抚顺模拟)(1)请写出Cr原子基态的电子排布式:
(2010?抚顺模拟)(1)请写出Cr原子基态的电子排布式:查看答案和解析>>
科目:高中化学 来源:2012届山西省高二下学期期中考试化学试卷 题型:填空题
(9分)请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有 种。
(2)请写出Cr元素的核外电子排布式 。
(3)某元素的正三价离子的3d能级为半充满,该元素的元素名称为 ,其单质在一定条件下能与S反应,试写出该反应的化学方程式 。
(4)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布图为 。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
钛已作为常用金属铁、铝后的第三金属,我国钛矿储量丰富,对它的应用研究是目前科学研究的前沿之一。
(1)请写出铝原子的基态电子排布式:___________________。
(2)X+、Y-、Z-与Al3+具有相同的电子层结构,则下列说法正确的是___________。
A.元素第一电离能:X> Al
B.电负性:Z >Y
C.氢化物稳定性:H2Y>HZ
D.H2Y中Y的杂化类型是sp3,键角小于109°28'
(3)某钙钛型复合氧化物如图1所示,以A原子为晶胞顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Ti、Fe时,这种化合物具有磁电阻效应。该钙钛型复合氧化物的化学式为________________
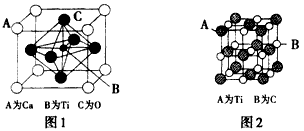
查看答案和解析>>
科目:高中化学 来源:2009-2010学年山东省淄博市高三(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com