
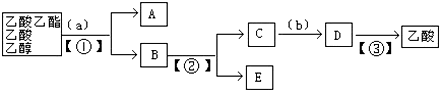
分析 由分离流程可知,分离乙酸乙酯、乙酸和乙醇的混合物,加入饱和碳酸钠溶液,乙酸乙酯不溶于饱和碳酸钠,采用分液的方法即可,水层中的乙酸钠要用硫酸反应得到乙酸,再蒸馏得到乙酸,以此来解答.
解答 解:(1)乙酸乙酯是不溶于水的物质,乙醇和乙酸均是易溶于水的,乙酸和乙醇的碳酸钠水溶液是互溶的,分离品乙酸乙酯、乙酸和乙醇的混合物,加入a为饱和碳酸钠溶液,实现酯与乙酸和乙醇的分离,分离油层和水层采用①分液的方法.对水层中的乙酸钠和乙醇进一步分离时应采取②蒸馏操作分离出乙醇,然后水层中的乙酸钠,根据强酸制弱酸,要用试剂b浓硫酸反应得到乙酸,再③蒸馏得到乙酸,
故答案为:饱和Na2CO3溶液;分液;蒸馏;蒸馏;
(2)由上述分析可知,A为CH3COOCH2CH3,E为CH3CH2OH,故答案为:CH3COOCH2CH3;CH3CH2OH;
无水碳酸钠粉末是一种良好的吸水剂,可以除掉乙酸乙酯中混有的少量水,故答案为:除去乙酸乙酯中混有的少量水;
(3)F与乙酸乙酯互为同分异构体,它能跟NaHCO3反应放出CO2,则F含-COOH,丙基有2种,则丁酸有2种,核磁共振仪处理能得到三种峰的是(CH3)2CHCOOH,其峰的面积之比为6:1:1,
故答案为:2;(CH3)2CHCOOH;6:1:1;
(4)苯甲酸的溶解度受温度影响大,室温下,苯甲酸的溶解度较小,温度升高,苯甲酸的溶解度增大,所以升温有利于提高苯甲酸的溶解度,在过滤时要趁热过滤除去泥沙,可以减少过滤时苯甲酸的损失,待过滤完则静置、缓慢冷却至室温,使苯甲酸以晶体形式析出.
故答案为:加热溶解、热过滤、冷却结晶.
点评 本题考查混合物分离提纯的实验设计,为高频考点,侧重于有机物知识的综合应用,为高频考点,把握混合物分离流程、分离方法及发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 物质 | HF | H2CO3 | HClO |
| 电离平衡常数(Ka) | 7.2×10-4 | Kal=4.4×10-7 Ka2=4.7×10-11 | 3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是甲醛 | B. | 可能是乙醛 | ||
| C. | 混合物中二者的质量比是1:3 | D. | 不可能有此种醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.1(m+n)g | B. | 14.2g | C. | 17.4g | D. | 20.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH2-CH2-CH2-CH3 | B. | HC≡C-CH2-CH2-CH2-CH3 | ||
| C. |  | D. | 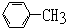 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
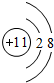
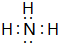 ,D单质能与水反应化学方程式是2Na+2H2O=2NaOH+H2↑.
,D单质能与水反应化学方程式是2Na+2H2O=2NaOH+H2↑.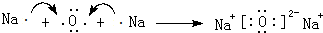 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑥ | B. | ②④⑤ | C. | ①②③ | D. | ④⑥⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com