

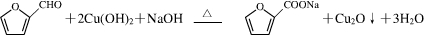
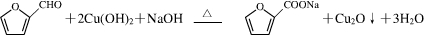


 .化合物
.化合物 是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以
是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以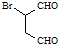 和
和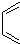 为原料合成该化合物(用合成路线流程图表示,并注明反应条件).合成路线流程图示例如下:
为原料合成该化合物(用合成路线流程图表示,并注明反应条件).合成路线流程图示例如下:
 可发生催化氧化生成
可发生催化氧化生成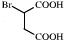 ,然后发生消去反应生成
,然后发生消去反应生成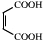 ,然后发生取代反应生成
,然后发生取代反应生成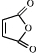 ,进而与
,进而与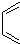 作用可生成目标物.
作用可生成目标物. ,根据D的结构简式可知,化合物D中含氧官能团的名称为酯基、羟基,
,根据D的结构简式可知,化合物D中含氧官能团的名称为酯基、羟基,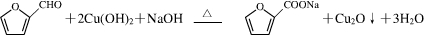 ,
,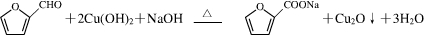 ;
; ,
, ;
;  可发生催化氧化生成
可发生催化氧化生成 ,然后发生消去反应生成
,然后发生消去反应生成 ,然后发生取代反应生成
,然后发生取代反应生成 ,进而与
,进而与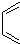 作用可生成目标物,反应流程为
作用可生成目标物,反应流程为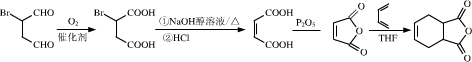 ,
, .
.

 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
(2013?江苏三模)下表为六种短周期元素的部分性质.
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
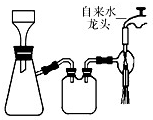 (2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下:
(2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com