
【题目】下列属于碱性氧化物的是( )
A.CaO
B.Na2O2
C.SiO2
D.Mn2O7
科目:高中化学 来源: 题型:
【题目】能说明BF3分子的四个原子在同一平面的理由是( )
A. 三个B—F键的键能相同 B. 三个B—F键的键长相同
C. 任意两个B—F键之间的夹角为120° D. 三个B—F键为极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2Fe2+ +Br2 = 2Fe3+ + 2Br-;2 Br- + Cl2 = Br2 + 2Cl-;2Fe3+ + 2I-= 2Fe2+ + I2。向 FeI2、FeBr2 的 混合溶液中通入 Cl2,溶液中某些离子的物质的量 n(离子)随通入 Cl2 的物质的量 n(Cl2)变化如图所示。则下列有关说法中不正确的是( )
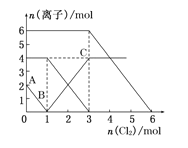
A. 还原性:I>Fe2+>Br
B. 原溶液中:n(Fe2+):n(I):n(Br)=2:1:3
C. 原混合溶液中 FeBr2 的物质的量为 6 mol
D. 当通入 2mol Cl2 时,溶液中已发生的离子反应可表示为:2Fe2++2I+2Cl2═2Fe3++I2+4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 0.1molSiO2晶体中含有Si-O键的数目为0.2NA
B. 56g铁粉与高温水蒸气反应,生成H2数目为1.5NA
C. 标准状况下,22.4 LCl2溶于水,转移电子数为NA
D. 18gH218O和D2O的混合物中,所含中子数为9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪种物质所含原子数与0.2 mol H3PO4所含原子数相等( )
A.0.4 mol H2O2B.0.2 mol H2SO4
C.0.9 mol NaClD.0.3 mol HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以柏林绿Fe[Fe(CN)6]为代表的新型可充电钠离子电池,其放电工作原理如图所示。下列说法错误的是

A. 放电时,正极反应为Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6]
B. 充电时,Mo(钼)箔接电源的负极
C. 充电时,Na+通过交换膜从左室移向右室
D. 外电路中通过0.2mol电子的电量时,负极质量变化为2.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中正确的是( )
A.化合反应一定是氧化还原反应
B.氧化还原反应的本质是元素化合价的升降
C.金属单质在化学反应中一定作还原剂
D.失电子的反应物在反应中作还原剂,反应中被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的钙离子、镁离子、硫酸根离子及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)第①步中,操作A是__________,第⑤步中,操作B是__________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)____________________________。
(3)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因是_________________________。
(4)判断氯化钡已过量的方法是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com