
| 1.2mol |
| 0.2mol |
| 1.2mol×2 |
| 0.2mol |
| 12 |
| 4 |
 ,
, .
.


科目:高中化学 来源: 题型:
| A、电解精炼铜时,若转移了NA个电子,则阴极析出32g铜 |
| B、标准状态下,33.6L氟化氢中含有1.5NA个氟化氢分子 |
| C、0.1mol/L的Al2(SO4)3溶液中,Al3+的数目小于0.2NA |
| D、1mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答:| T/K | 298 | 398 | 498 | … |
| K/(mol?L-1)2 | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:
 5种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水.
5种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水.| 阳离子 | Na+ Al3+Fe3+ Cu2+ Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,组成一个原电池.
如图所示,组成一个原电池.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
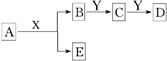 中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去).下列推断正确的是( )
中学化学中,常见无机物A、B、C、D、E、X、Y存在如下图转化关系(部分生成物和反应条件略去).下列推断正确的是( )| A、若A是CaC2,X是H2O,则Y一定是溴水 |
| B、若A是金属钠,X是H2O,则E一定能还原Fe2O3 |
| C、若Y是NaOH,C是白色沉淀,则A与X一定发生置换反应 |
| D、若Y是氧气,D是氧化物,则A与X一定发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐类水解是中和反应的逆反应 |
| B、盐类水解过程是吸热过程 |
| C、含有弱酸根盐的水溶液一定显碱性 |
| D、盐溶液的酸碱性主要决定于形成盐的酸和碱的相对强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com