
| A£® | Ö»ŅŖŌŚŹŅÄŚ·ÅŅ»ÅčĖ® | |
| B£® | ĻņµŲŹĘµĶµÄµŲ·½³·Ąė | |
| C£® | ¹Ū²ģ·ēĻņ£¬Ė³·ē³·Ąė | |
| D£® | ÓĆŹŖĆ«½ķ»ņÕŗÓŠČõ¼īŠŌČÜŅŗµÄĆ«½ķĪę×”æŚ±Ē³·Ąė |
·ÖĪö øł¾ŻĀČĘųµÄĪļĄķŠŌÖŹ”¢»ÆѧŠŌÖŹÅŠ¶Ļ£®ĀČĘųŹĒŅ»ÖÖÓŠ¶¾”¢ĆܶȓóÓŚæÕĘųĆܶȵÄĘųĢ壬ÄÜŗĶ¼īŠŌČÜŅŗ·“Ó¦”¢ÄÜŗĶĖ®·“Ó¦£¬1Ģå»żµÄĖ®ÄÜČܽā2Ģå»żµÄĀČĘų£®
½ā“š ½ā£ŗA”¢ĖäČ»ĀČĘųÄÜŗĶĖ®·“Ó¦£¬ĒŅĀČĘųµÄČܽāŠŌ²»“ó£¬ŹŅÄŚ·ÅŅ»ÅčĖ®²»ÄÜĪüŹÕ“óĮæµÄĀČĘų£¬¹ŹA“ķĪó£»
B”¢ĀČĘųµÄĆܶȓóÓŚæÕĘųµÄĆÜ¶Č£¬ĒŅĀČĘųÓŠ¶¾£¬¹ŹB“ķĪó£»
C”¢øł¾Ż·ēĻņ£¬ĻņÄę·ē·½Ļņ³·Ąė£¬¹ŹC“ķĪó£»
D”¢Cl2+H2O=HCl+HClO”¢2HCl+Na2CO3=2NaCl+H2O+CO2”ü£¬ĖłŅŌæÉÓĆŹŖĆ«½ķ»ņÕŗÓŠ“æ¼īĖ®µÄĆ«½ķĪę×”æŚ±Ē³·Ąė£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éµÄŹĒĀČĘųµÄĪļĄķŠŌÖŹŗĶ»ÆѧŠŌÖŹ£¬»ÆѧŌ“ÓŚÉś»ī£¬“Ó»ÆѧŹÓ½Ē¹Ū²ģÉś»ī£¬°Ń»ÆѧÖŖŹ¶Ó¦ÓĆÓŚÉś»ī£¬ŅŖѧŅŌÖĀÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĘČ”8.0 g CuSO4£¬¼ÓČė500 mLĖ® | |
| B£® | ³ĘČ”7.68 g CuSO4£¬¼ÓČė480 mLĖ® | |
| C£® | ³ĘČ”12.5 g CuSO4•5H2O£¬¼ÓĖ®Åä³É500 mLČÜŅŗ | |
| D£® | ³ĘČ”12.0 g CuSO4•5H2O£¬¼ÓĖ®Åä³É480 mLČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
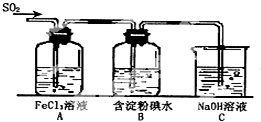 ijŠĖȤŠ”×éŃŠ¾æSO2ĘųĢ廹ŌFe3+”¢I2£¬ĖūĆĒŹ¹ÓƵÄŅ©Ę·ŗĶ×°ÖĆČēĶ¼ĖłŹ¾£ŗ
ijŠĖȤŠ”×éŃŠ¾æSO2ĘųĢ廹ŌFe3+”¢I2£¬ĖūĆĒŹ¹ÓƵÄŅ©Ę·ŗĶ×°ÖĆČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 0.1 mol•L-1 CH3COONaČÜŅŗÓė0.1 mol•L-1 HClČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØNa+£©=c£ØCl-£©£¾c£ØCH3COO-£©=c£ØOH-£© | |
| B£® | 0.1 mol•L-1 NH4ClČÜŅŗÓė0.1 mol•L-1°±Ė®µČĢå»ż»ģŗĻ£ØpH£¾7£©£ŗc£ØNH3•H2O£©£¾c£ØNH${\;}_{4}^{+}$£©£¾c£ØCl-£©£¾c£ØOH-£© | |
| C£® | 0.1 mol•L-1 Na2CO3ČÜŅŗÓė0.1 mol•L-1 NaHCO3ČÜŅŗµČĢå»ż»ģŗĻ£ŗ$\frac{2}{3}$c£ØNa+£©=c£ØCO${\;}_{3}^{2-}$£©+c£ØHCO${\;}_{3}^{-}$£©+c£ØH2CO3£© | |
| D£® | 0.1 mol•L-1 Na2C2O4ČÜŅŗÓė0.1 mol•L-1 HClČÜŅŗµČĢå»ż»ģŗĻ£ØH2C2O4ĪŖ¶žŌŖČõĖį£©£ŗ2c£ØC2O${\;}_{4}^{2-}$£©+c£ØHC2O${\;}_{4}^{-}$£©+c£ØOH-£©=c£ØNa+£©+c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬44 g C3H8ÖŠŗ¬ÓŠµÄĢ¼Ģ¼µ„¼üŹżĪŖ3NA | |
| B£® | 1molōĒ»łÖŠµē×ÓŹżĪŖ9NA | |
| C£® | ŹŅĪĀĻĀ£¬21.0gŅŅĻ©ŗĶ¶”Ļ©µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżÄæĪŖ1.5NA | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4L ¼×“¼ÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ1.0NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
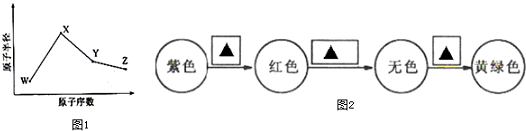
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com