
【题目】奥司他韦是一种高效、高选择性神经氨酸酶抑制剂,是目前治疗流感的最常用药物之一,是公认的抗禽流感、甲型H1N1等病毒最有效的药物之一. 也是国家的战略储备药物。也有专家尝试使用奥司他韦作为抗新现冠状病毒肺炎药物。奥司他韦的合成路线如下:
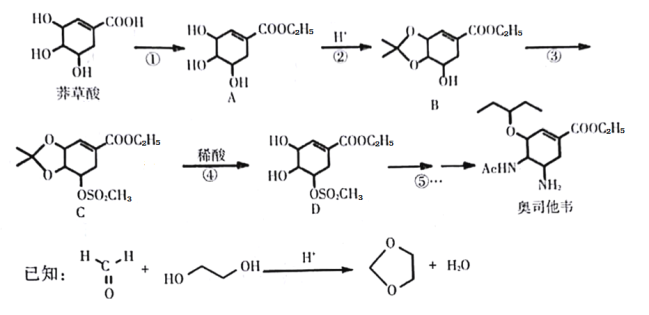
回答下列问题:
(1)莽草酸的含氧官能团名称为:___________
反应③的反应类型:__________________。
(2)反应①的反应试剂和反应条件:________________________________。
(3)请写出反应②的化学方程式:__________________________________。
(4)芳香化合物X是B的同分异构体,则符合官能团只含酚羟基的X有_____种。
(5)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。C中有_____个手性碳。
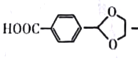
(6)设计由对甲基苯甲醛![]() 制备对醛基苯甲酸
制备对醛基苯甲酸![]() 的合成路线如下图所示。
的合成路线如下图所示。
![]()
![]() M
M![]()
![]()
![]()
写出M结构简式__________________,条件1为_______________________。
【答案】羟基、羧基 取代反应 乙醇、浓硫酸,加热 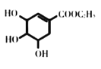 +
+![]()
![]()
 +H2O 17 3
+H2O 17 3 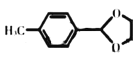 高锰酸钾
高锰酸钾
【解析】
莽草酸与乙醇在浓硫酸作催化剂加热条件下发生酯化反应生成A,结合已知信息,A与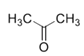 在酸性条件下反应生成B,B与HO-SO2CH3发生取代反应生成C,C加入稀酸作用下生成D在经过一系列反应最终得到奥斯他韦,据此分析解答。
在酸性条件下反应生成B,B与HO-SO2CH3发生取代反应生成C,C加入稀酸作用下生成D在经过一系列反应最终得到奥斯他韦,据此分析解答。
(1)莽草酸的结构简式为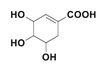 ,含氧官能团名称有:羟基、羧基;根据分析反应③的反应类型为取代反应;
,含氧官能团名称有:羟基、羧基;根据分析反应③的反应类型为取代反应;
(2)根据分析,反应①为莽草酸与乙醇在浓硫酸作催化剂加热条件下发生酯化反应生成A,反应试剂和反应条件:乙醇、浓硫酸,加热;
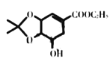
(3)根据分析,反应②为A与 在酸性条件下反应生成B的化学方程式:
在酸性条件下反应生成B的化学方程式: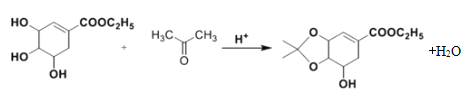 ;
;
(4)B的结构简式为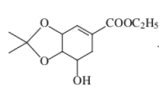 ,芳香化合物X是B的同分异构体,则X中有苯环,官能团只含酚羟基,则X中有5个-OH,并直接连在苯环上,则X为
,芳香化合物X是B的同分异构体,则X中有苯环,官能团只含酚羟基,则X中有5个-OH,并直接连在苯环上,则X为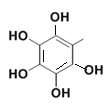 和-C6H13,根据题意
和-C6H13,根据题意 在X的结构中为一个固定原子团结构,可将
在X的结构中为一个固定原子团结构,可将 看作卤素原子,如Cl原子,则该有机物可写为C6H13Cl(Cl代表
看作卤素原子,如Cl原子,则该有机物可写为C6H13Cl(Cl代表 原子团),故同分异构体情况分别如下:正己烷分子中含有3类氢原子,2-甲基戊烷分子中含有5类氢原子,3-甲基戊烷分子中含有4类氢原子,2,2-二甲基丁烷分子中含有3类氢原子,2,3-二甲基丁烷分子中含有2类氢原子,则该有机物符合要求的同分异构体的数目为17个;
原子团),故同分异构体情况分别如下:正己烷分子中含有3类氢原子,2-甲基戊烷分子中含有5类氢原子,3-甲基戊烷分子中含有4类氢原子,2,2-二甲基丁烷分子中含有3类氢原子,2,3-二甲基丁烷分子中含有2类氢原子,则该有机物符合要求的同分异构体的数目为17个;
(5)碳原子上连有4个不同的原子或基团时,该碳称为手性碳;C的结构简式为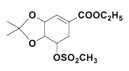 ,其中是手性碳的如图所示
,其中是手性碳的如图所示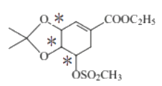 ,有3个手性碳;
,有3个手性碳;
(6)根据已知信息,可以推测出M为: ;条件1是将苯环上的甲基氧化成羧基,故条件1为高锰酸钾溶液。
;条件1是将苯环上的甲基氧化成羧基,故条件1为高锰酸钾溶液。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述不正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述不正确的是( )
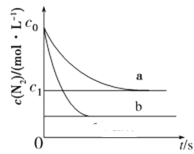
A.温度T下,该反应的平衡常数![]()
B.温度T下,随着反应的进行,混合气体的密度不变
C.曲线b对应的条件改变可能是增大压强
D.若曲线b对应的条件改变是温度,可判断该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构进行如下各实验:
①6.0g有机物A在一定条件下完全分解,只生成3.36L(标准状况)一氧化碳和XgH2O。
②A的蒸气在标准状况下的密度为5.357g/L
③中和0.24g有机物A,消耗0.20mol/L的氢氧化钠溶液20.00mL;0.01mol物质A完全转化为酯,需乙醇0.92g;0.01mol物质A能与足量钠反应放出0.336L标准状况下的氢气。试确定:
(1)生成水的质量为____g。
(2)A的式量___,A的化学式_____。
(3)试推测A的结构简式。______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与我们的生活密切相关,请回答:
(1)在生活中要注意饮食平衡,蛋白质属于_______(填序号,下同)食物,番茄属于______食物;①酸性 ②碱性
(2)有四种常见药物①阿司匹林、②青霉素、③胃舒平、④麻黄碱. 某同学胃酸过多,应该服用______(填序号,下同);从用药安全角度考虑,使用前要进行皮肤敏感性测试的是_____;由于具有兴奋作用,国际奥委会严禁运动员服用的是_________;
(3)苹果汁是人们喜爱的饮品,由于其中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色,若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有________(填序号);①氧化性 ②还原性 ③碱性 ④酸性
(4)食用植物油进入人体后,在酶的作用下水解为高级脂肪酸和_________(写名称),进而被氧化成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料;
(5)硫酸亚铁可用于治疗缺铁性贫血,某贫血患者每天须补充1.4g铁元素,则服用的药物中含硫酸亚铁的质量至少为_________g;
(6)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(﹣NH2)和____(写结构简式或名称).人体中共有二十多种氨基酸,其中人体自身________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸;
(7)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水.写出葡萄糖在体内被氧化的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟用下图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁粉、稀硫酸、氢氧化钠溶液。
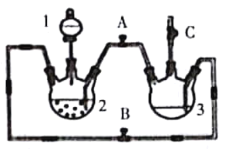
(1)稀硫酸应放在_________中(填写仪器名称).
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关______、打开开关_________就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由____________。
(3)该实验使用铁粉,除反应速率可能太快外,还可能会造成的不良后果是_______________。
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](该晶体比一般亚铁盐稳定 ,不易被氧化,易溶于水,不溶于乙醇),用如图所示的装置抽滤,与普通漏斗过滤相比,抽滤的优点是_____________________________。
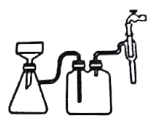
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是____。
A.用冷水洗
B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗
D.用90%的乙醇溶液洗
②测定摩尔盐中铁的含量。称取ag产品于锥形瓶中,溶解后加稀硫酸酸化,用c mol·L-1的酸性KMnO4溶液滴定至终点,滴定终点的现象是_______________。到达终点消耗KMnO4的体积为VmL,则该晶体中铁的质量分数的表达式为_______________________(用字母a,c,V 表示)。
③实验室可用______( 填试剂名称)检验Fe2+存在,出现特征蓝色沉淀的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”。钛铁矿(主要成分为FeTiO3,含少量Fe2O3、SiO2等杂质)可用来制备TiO2,同时得到副产品绿矾(FeSO4·7H2O),工艺流程如图所示:
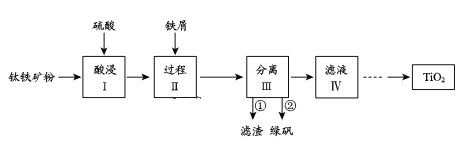
己知:①FeTiO3+2H2SO4=FeSO4+TiOSO4+2H2O
②TiO2+易水解,只能存在于强酸性溶液中
(1)酸浸I中Fe2O3与稀硫酸反应的离子方程式:_____。
(2)过程II中加入适量铁屑的目的是____。
(3)分离III中步骤②得到绿矾的操作是_____。
(4)由滤液IV提取TiO2的过程如下:
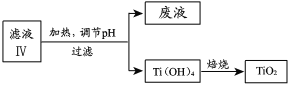
①请用化学平衡移动原理解释滤液加热煮沸的目的:______。
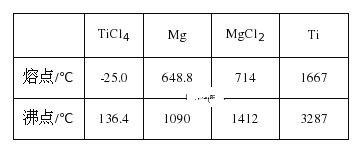
②由2Mg+TiCl4→Ti+2MgCl2反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据如表信息,需加热的温度略高于___℃即可。
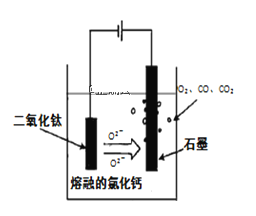
③电解TiO2制备钛的方法如图所示。该方法由于具备生产过程简化、生产成本低、产品质量高、环境友好等诸多优点而引人注目。已知TiO2熔融状态下不发生电离,电解时阴极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图所示装置可以模拟铁的电化学腐蚀。下列说法中,正确的是

A. 若X为碳棒,开关K置于M处可以减缓铁的腐蚀
B. 若X为铜棒,开关K置于N处可以加快铁的腐蚀
C. 若X为碳棒,开关K置于M处,则为牺牲阳极的阴极保护法
D. 若X为碳棒,开关K置于N处,则为外加电流的阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是( )
A.54g H2O中含有3NA个氢原子
B.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
C.标准状况下,NA个H2O分子所占的体积约为22.4L
D.1mol CO2和NO2的混合物中含的氧原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL Fe2(SO4)3溶液中含Fe3+56g,在该溶液中加入1mol/LBaCl2溶液300mL,反应后溶液中SO42-的物质的量浓度是(忽略混合后溶液的体积变化) ( )
A.7.5mol/LB.5mol/LC.6mol/LD.2.4mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com