
欲使1L 0.5mol/L的NaOH溶液的浓度增大一倍,可采取的合理措施是
A.加入20g 固体NaOH,搅拌、溶解;
B.将溶液加热浓缩至0.2L;
C.加入10mol/L的NaOH溶液0.1 L,再稀释至1.5 L;
D.加入1 L 1.5 mol/L的NaOH溶液混合均匀。
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
下列有关实验的做法错误的是
A.分液时,分液漏斗中的上层液体应由上口倒出
B.用加热的方法可区分碳酸钠和碳酸氢钠两种固体
C.用渗析的方法可除去Fe(OH)3胶体中混有的Cl-
D.加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是制取气体的一种装置,能用此装置制取气体并能“随开随用,随关随停”的是( )
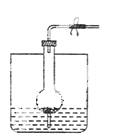
A.碱石灰与浓氨水制NH3 B.铝片与烧碱溶液制H2
C.电石与饱和食盐水制乙炔(C2H2) D.亚硫酸钠固体与75%的硫酸制SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下图所示的装置制取乙酸乙酯。
 (1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,其操作步骤为 ____
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,其操作步骤为 ____ _______ ____________________________________,然后轻轻振荡试管使之混合均匀。
_______ ____________________________________,然后轻轻振荡试管使之混合均匀。
(2)装置中通蒸气的导管要插在饱和的Na2CO3溶液的液面上而不能插入溶液中,目的是防止溶液的倒吸。造成倒吸的原因是_______________________。
(3)浓硫酸的作用是:①__________________;②____________________。
(4)图中右边试管中试剂是_______________。
(5)分离得到乙酸乙酯的方法是__________,分离需要的玻璃仪器是____________________。
(6)若加的是C2H518OH写出制乙酸乙酯的方程式____________________________________。
(7)写出乙酸与碳酸氢钠反应方程式_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
丙酮(C3H6O)通常是无色液体,与水混溶,密度小于1g·mL-1,沸点约为56℃。要从水与丙酮的混合物中分离出丙酮,下列方法中最合理的是
A.蒸馏, B.分液, C.过滤, D.蒸发。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)摩尔是国际单位制中七个基本单位之一,对应的物理量是 ;
(2)1mol粒子集体所含的粒子数与 kg12C所含的碳原子数相等;
(3)1mol物质的质量(以 为单位)数值上等于该物质的相对分子质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或说法错误的是
A.蒸发时,蒸发皿中固体不能蒸干才停止加热
B.蒸馏时,温度计水银球应靠近蒸馏烧瓶的支管口处
C.分液时,分液漏斗中下层液体从下口放出 ,上层液体从上口倒出
,上层液体从上口倒出
D.焰色反应时,用稀硫酸洗 净铂丝,并在火焰上灼烧至无色
净铂丝,并在火焰上灼烧至无色
查看答案和解析>>
科目:高中化学 来源: 题型:
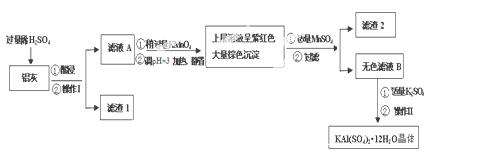
明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al 、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:
回答下列问题:
(1)明矾净水的原理是(用离子方程表示)
(2)操作Ⅰ是 ,操作Ⅱ是蒸发浓缩、 、过滤、 干燥。
(3)检验滤液A中是否存在Fe2+的方法是 (只用一种试剂)
(4)在滤液A中加入高锰酸钾的目的是 ,发生反应的离子方程式为(该条件下Fe2+ 转化为Fe3+,MnO4- 转化为Mn2+) 。
已知:生成氢氧化物沉淀的pH如下表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释调pH=3的目的 。
(5)己知:在pH=3、加热条件下,MnO4- 可与Mn2+反应生成MnO2。加入MnSO4发生反应的离子方程式为: 。滤渣2含有的物质是 。
(6)以Al和NiO(OH)为电极,KOH溶液为电解液可组成新型、高效电池,充放电过程中,发生Ni(OH)2与NiO(OH)之间的转化,写出放电时电池反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
舱外航天服每套总重量约 120 公斤,造价 3000 万元人民币左右。舱外航天服可为航天员出舱活动提
供适当的大气压力、足够的氧气、适宜的温湿度,以保障航天员的生命活动需要;航天服具有足够的强度,
防止辐射、微流量和空间碎片对航天员的伤害,保证航天员的工作能力;航天服还能提供可靠工效保障及
遥测通信保障等。制作这种宇航服的材料以氨纶和尼龙为主。其中尼龙-1010 的结构简式为

 下列有关尼龙-1010 的说法正确的是
下列有关尼龙-1010 的说法正确的是
( )
A. 尼龙-1010 是通过加聚反应制成的
尼龙-1010 是通过加聚反应制成的
B.尼龙-1010 的单体是 H2N (CH2)10 NHCO(CH2)8COOH
C.尼龙-1010 是通过缩聚反应制成的
D.制作舱外航天服的材料要质轻,方便在舱外行走
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com