
����Ŀ����A201�ʹ�������FeO������CoO��Al2O3��CaO�����Ʊ����ƣ�Fe2O3H2O����
��1��CoO��Co�Ļ��ϼ�Ϊ ��
��2���ϴ����е����������������ǿ�ᷴӦ�������ʵ�����FeO��Al2O3�ֱ���������ϡHNO3��Ӧ������HNO3�����ʵ���֮��Ϊ ��
��3����ҵ���÷ϴ����Ʊ�����ʱ�ж�����裮
�ٽ��ϴ������з��飬��Ŀ���� ��
���������ữ���ټ���NaClO��Һ��Fe2+����������ʱ������Ӧ�����ӷ���ʽΪ ��
�۾���һϵ�в����ɵõ����ƣ���֪���Ʋ�����ˮ��ʹ���ƴ���Һ�з�����������еIJ����У��õ��IJ���������©���� ��
���𰸡�
��1��+2
��2��5��9
��3������Ӧ�ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ�2Fe2++ClO��+2H+=2Fe3++Cl��+H2O�����������ձ�
���������⣺��1��CoO��Co�Ļ��ϼ�Ϊ+2�����Դ��ǣ�+2����2��3FeO+10HNO3=3Fe��NO3��3+NO��+5H2O���μӷ�Ӧ��������10mol��Al2O3�ֱ���������ϡHNO3��Ӧ������ʽΪ��Al2O3+6HNO3=2Al��NO3��3+3H2O����1molAl2O3����6mol�����ᣬ���Ե����ʵ�����FeO��Al2O3�ֱ���������ϡHNO3��Ӧ������HNO3�����ʵ���֮��Ϊ ![]() ��6=5��9�����Դ��ǣ�5��9����3���ٽ��ϴ������з��飬��Ŀ��������Ӧ�ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ����Դ��ǣ�����Ӧ�ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ����������ữ���ټ���NaClO��Һ��Fe2+����������ʱ������Ӧ�����ӷ���ʽΪ2Fe2++ClO��+2H+=2Fe3++Cl��+H2O�����Դ��ǣ�2Fe2++ClO��+2H+=2Fe3++Cl��+H2O���۹����õ��IJ���������©�������������ձ������Դ��ǣ����������ձ���
��6=5��9�����Դ��ǣ�5��9����3���ٽ��ϴ������з��飬��Ŀ��������Ӧ�ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ����Դ��ǣ�����Ӧ�ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������ʣ����������ữ���ټ���NaClO��Һ��Fe2+����������ʱ������Ӧ�����ӷ���ʽΪ2Fe2++ClO��+2H+=2Fe3++Cl��+H2O�����Դ��ǣ�2Fe2++ClO��+2H+=2Fe3++Cl��+H2O���۹����õ��IJ���������©�������������ձ������Դ��ǣ����������ձ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д����ȷ���ǣ� ��
A.�ڿ����м����ƣ�2Na+O2 ![]() Na2O2
Na2O2
B.��FeCl3��Һ�еμӵ��۵⻯����Һ��2Fe3++2I���T2Fe2++I2
C.����ˮ������Ӧ��2Fe+3H2O��g�� ![]() Fe2O3+3H2
Fe2O3+3H2
D.��������Һ�е���ϡ���Na2SiO3+2HCl�TH2SiO3�����壩+2NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ͼ��ʾװ����ȡ��ˮ���������ʵ�飮 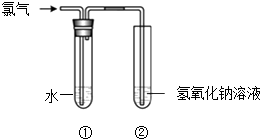
��1��װ�â��з�Ӧ�Ļ�ѧ����ʽ�� ��
��2��ʵ�����һ��ʱ���װ�â�����Һ�ʻ���ɫ���ɴ�˵������Һ��һ�����е����������ѧʽ����
��3��ȡ����װ�â��е���Һ������ɫʯ����ֽ�ϣ���ֽ�ȱ�����ɫ��˵����ˮ����������ţ��� a�����Ժ�Ư���� b�����Ժ�Ư����
��4����֪������ͨ���ȵ�����������Һ�У��ɷ������·�Ӧ��Cl2+NaOH��A+NaClO3+H2O��δ��ƽ�����У�A�Ļ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.����Ƥ�����Ҫ�ɷ��ǵ�����
B.��Ȼ������ˮ������ղ�������-������
C.Ƥ�����ƹ�����ʹ�õ�K2Cr2O7��ʹ����������
D.��Ƥ����������ʱ���ս���ë����ζ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں˴Ź��������г�������壬����ԭ�Ӹ���֮��Ϊ3��2�Ļ������ǣ� ��
A.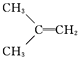
B.![]()
C.![]()
D.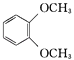
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Fe2O3��s��+ ![]() C��s���T
C��s���T ![]() CO2��g��+2Fe��s����H=+234.1kJ/mol
CO2��g��+2Fe��s����H=+234.1kJ/mol
C��s��+O2��g���TCO2��g����H=��393.5kJ/mol
��2Fe��s��+ ![]() O2��g���TFe2O3��s���ġ�H�ǣ� ��
O2��g���TFe2O3��s���ġ�H�ǣ� ��
A.��824.4 kJ/mol
B.��627.6 kJ/mol
C.��744.7 kJ/mol
D.��169.4 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������µķ��ӻ������У�VSEPRģ������������ӵ����幹������һ�µ��ǣ� ��
A.NF3
B.![]()
C.SO3
D.H3O+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��У�����ܵ����¼�ý�峣�б����������������˺���ԭ��֮һ�dz���ʹ���˱����ױ����л��ܼ��������й�˵����ȷ���ǣ� ��
A.�ױ��ķ���ʽΪ�� 
B.�ױ�����������ԭ�Ӷ�����ͬһƽ��
C.�ױ���һ��ȡ������5��ͬ���칹�壬���ǵ��۵㡢�е������ͬ
D.�ױ��ͱ���Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������У�����ԭ�Ӷ����������Ϊ8���ӽṹ���� (�� )
A. BeCl2B. CH4C. HClD. PCl3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com