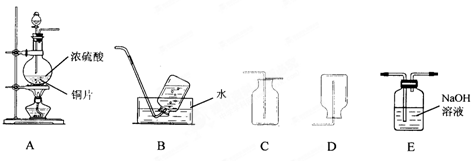
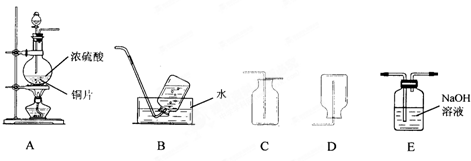
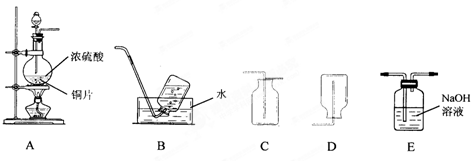
硫酸是一种重要的化学试剂.某实验小组的同学利用浓硫酸进行如下实验.请按要求回答下列问题.

I.制取二氧化疏并探究其性质
(1)装置A中发生反应的化学方程式为
.上述装置中适于收集二氧化硫气体的是(填字母)
.
(2)将一收集满二氧化硫气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是
.
(3)上述实验所产生的二氧化硫尾气可选用E装置来吸收,该反应的化学方程式为
.
Ⅱ.处理含正六价铬的废水样液(+6价Cr的含量为78mg/L).实验步骤如下:
①取1L废水加入一定量1.8mol/LH
2SO
4溶液使样液酸化
②加入一定量的绿矾(FeSO
4?7H
2O),将正六价铬转化为正三价铬离子
③加入过量的石灰水,使正三价铬离子转化为Cr(OH)
3沉淀
④过滤,除去沉淀物
(1)配制步骤①中所需H
2SO
4溶液100mL,需用18mol/L H
2SO
4溶液的体积是
mL.
(2)步骤②中反应的离子方程式为14H
++Cr
2O
72-+6Fe
2+═2Cr
3++6Fe
3++7H
2O此反应中氧化剂和还原剂物质的量之比为
.
(3)步骤④分离出的沉淀物中含有Cr(OH)
3、CaSO
4和
.
(4)处理1L该废水样液至少需要绿矾
g.

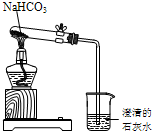 某实验小组的同学利用下图所示的装置进行NaHCO3的受热分解实验.请回答下列问题:
某实验小组的同学利用下图所示的装置进行NaHCO3的受热分解实验.请回答下列问题:

 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案