
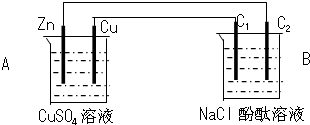
分析 (1)有外加电源的是电解池,没有外加电源的是原电池或者根据原电池和电解池的构成条件来回答;
(2)原电池中活泼金属锌是负极,锌失电子生成锌离子,金属铜是正极,正极上是电解质里的阳离子得电子的还原反应;
(3)石墨棒C1和原电池正极相连为电解池阳极,石墨棒C2和原电池的负极相连,氢离子得电子发生还原反应,据此回答;
(4)根据电子守恒定律结合电极反应式进行计算回答.
解答 解:(1)装置A符合原电池的构成条件:两个活泼性不同的电极,属于原电池,Zn失电子族负极,装置B符合电解池的构成条件,属于电解池;
故答案为:原电池;电解池;
(2)A中金属锌是负极,电极反应为Zn-2e-=Zn2+,金属铜是正极,正极反应是:Cu2++2e-→Cu,故答案为:负;Zn-2e-=Zn2+;
(3)石墨棒C1和原电池正极相连为电解池阳极,溶液中氯离子失电子发生氧化反应生成氯气,电极反应为:2Cl--2e-=Cl2↑,石墨棒C2和原电池的负极相连,是阴极,氢离子放电,所以氢离子浓度减小而氢氧根浓度增大,碱性增强,使酚酞变红,
故答案为:阳;2Cl--2e-=Cl2↑;电极上有气泡产生,无色溶液变红色;
(4)C2极发生的电极反应为:2H++2e-→H2↑,析出224mL(即0.01mol)气体(标准状态)时,转移电子数是0.02mol,所以锌极转移电子也为0.02mol,根据电极反应:Zn-2e-→Zn2+,消耗金属锌0.01mol,质量是0.01mol×65g/mol=0.65g,故答案为:0.65.
点评 本题考查了原电池和电解池原理的应用,把握原电池和电解池的工作原理以及电子守恒原理,题目难度不大.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1s22s22p63s1→1s22s22p6 | |
| B. | N≡N(g)→N(g)+N(g) | |
| C. | 2p${\;}_{x}^{2}$2p${\;}_{y}^{1}$2p${\;}_{z}^{1}$→2p${\;}_{x}^{1}$2p${\;}_{y}^{1}$2p${\;}_{z}^{2}$ | |
| D. | 2H(g)→H-H(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向亚硫酸饱和溶液中通入适量氯气 | B. | 向硝酸银溶液通入少量HCl | ||
| C. | 向氢氧化钠溶液中通入少量Cl2 | D. | 向NaOH溶液中加入醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.44 s | B. | 1 s | C. | 1.33 s | D. | 2 s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| D. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(8x-2y) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳棒上放出氯气 | B. | 铁钉上放出氢气 | C. | 碳棒上放出氧气 | D. | 铁钉锈蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①③⑤ | C. | ①③④ | D. | ②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com