

| A. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| B. | 在镀件上电镀锌,用锌作阳极 | |
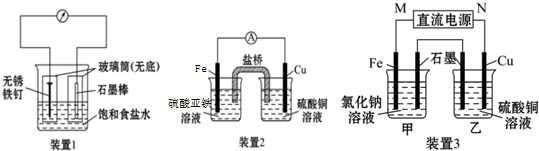
| C. | 用如图1装置生产家用消毒液(NaClO) | |
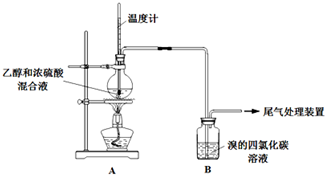
| D. | 用如图2装置为铅蓄电池充 |
分析 A.加热促进盐的水解,盐酸为挥发性酸;
B.电镀时镀层金属作阳极;
C.生产家用消毒液(NaClO)的原理是让电解氯化钠溶液生成的氯气和氢氧化钠之间发生反应即可;
D.充电时,外接电源的正极与铅蓄电池的正极相连.
解答 解:A.加热促进盐的水解,而且盐酸为挥发性酸,制备AlCl3、FeCl3、CuCl2发生水解生成盐酸,所以不能采用将溶液直接蒸干的方法,故A正确;
B.电镀时镀层金属作阳极,待镀金属作阴极,所以在镀件上电镀锌,用锌作阳极,故B正确;
C.生产家用消毒液(NaClO)的原理是让电解氯化钠溶液生成的氯气和氢氧化钠之间发生反应即可,氯离子在阳极失电子生成氯气,阴极上氢离子得电子生成氢气和氢氧根离子,氯气与氢氧根离子反应生成次氯酸钠,故C正确;
D.充电时,外接电源的正极与铅蓄电池的正极相连,PbO2为正极应该与正极相连,故D错误.
故选D.
点评 本题考查了盐的水解原理、原电池和电解池原理的应用,题目难度不大,注意把握影响水解平衡的因素、电极的判断和电极方程式的书写.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-二甲基丁烷 | B. | 2,3-二甲基-2-乙基己烷 | ||
| C. | 2,3-二甲基-4-乙基戊烷 | D. | 2,3,5-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO HNO3 | B. | CH2=CH2 CH3CHO | C. | Fe FeCL3 | D. | Si H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
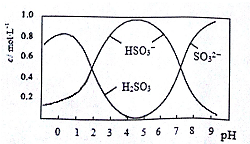
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | |
| Z | W | |
| T |
| A. | 氢化物稳定性Y比W强,是因为Y的氢化物中存在氢键 | |
| B. | XY2、XW2、ZY2熔沸点依次增大,都是由共价键形成的分子晶体 | |
| C. | 一定条件下,X单质能与ZY2反应生成Z单质,说明X的非金属性比Z强 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,钠能与T形成Na2T2化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 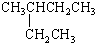 2-乙基丁烷 | B. | CH3CHBr2二溴乙烷 | ||
| C. |  2-甲基丁烯 | D. | 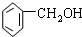 苯甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转化过程中,增大c(H+),平衡向正反应方向移动,CrO42-的转化率提高 | |
| B. | 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 | |
| C. | 若用绿矾(FeSO4•7H2O)(M=278)作还原剂,处理1L废水,至少需要917.4g | |
| D. | 常温下转化反应的平衡常数K=104,则转化后所得溶液的pH=1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com