

���� ��Ȼ�л��߷��ӻ�����A����ɫֲ�������õIJ����Ҫ������ֲ������ӻ����AΪ���ۣ����ͼ��ת����֪��C�ɷ�����������Ӧ����Aˮ������BΪ�����ǣ�B�����ƻ���Ӧ����CΪCH3CH2OH��DΪCH3CHO��EΪCH3COOH��FΪCH3COOCH2CH3���Դ������
��� �⣺��1����A����B�Ļ�ѧ����ʽΪ��C6H10O5��n+nH2O$\stackrel{����}{��}$nC6H12O6��
�ʴ�Ϊ����C6H10O5��n+nH2O$\stackrel{����}{��}$nC6H12O6��
��2��B��D�����еĹ�������ȩ��������B��ȩ���ķ���Ϊ��
��ȡһ֧�ྻ���Թܣ������м���B����Һ��
�ڵ���3������ͭ��Һ�������������������Һ���к���������ɫ������
�ۼ�����У����Կ����к�ɫ�������֣�
�ʴ�Ϊ��ȩ������ȡһ֧�ྻ���Թܣ������м���B����Һ���ڵ���3������ͭ��Һ�������������������Һ���к���������ɫ�������ۼ�����У����Կ����к�ɫ�������֣�
��3��A��B����ˮ�ⷴӦ��B��C�����ֽⷴӦ��C��D����������Ӧ��D��EΪ������Ӧ��C��E����������Ӧ����F��
�ʴ�Ϊ��ABD��
��4��C��D��������Ӧ�Ļ�ѧ����ʽΪ2C2H5OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
�ʴ�Ϊ��2C2H5OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
���� ���⿼���л�����ƶϼ��ϳɣ�Ϊ��Ƶ���㣬���ո߷��ӻ�����AΪ����Ϊ���Ĺؼ������ط������ƶ������Ŀ��飬ע���л���Ӧ���л�������ʣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧʵ���У�������Һ���Լ������ữ�������ữ�����Ĵ�ʩ����ȷ����
A. ���Լ���SO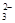 ������HNO3�ữ��BaCl2��Һ
������HNO3�ữ��BaCl2��Һ
B. Ϊ�����KMnO4��Һ�������������������Ὣ���ữ
C. ����ij��Һ���Ƿ�Cl�C����HNO3�ữ��AgNO3��Һ
D. ����FeCl2��Һʱͨ��������H2SO4�ữ����С��ˮ��̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 27 mg | B�� | 54 mg | C�� | 108 mg | D�� | 216 mg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����ȣ�SrSO4���������̻���մɹ�ҵ���������ǿ�������ʯ����Ҫ�ɷ֣�����Na2SO4��Һ����������Һ�������ã���ͼ�������ȵ��ܽ����ߣ�����˵����ȷ���ǣ�������
�����ȣ�SrSO4���������̻���մɹ�ҵ���������ǿ�������ʯ����Ҫ�ɷ֣�����Na2SO4��Һ����������Һ�������ã���ͼ�������ȵ��ܽ����ߣ�����˵����ȷ���ǣ�������| A�� | ͼ����a��c������ܶȻ���Ksp��a����Ksp��c�� | |
| B�� | 363Kʱ���ܶȻ�Ksp��SrSO4��=1.0��10-3.20 | |
| C�� | SrSO4���ܽ�����¶����߶����� | |
| D�� | 313Kʱ��b��Ϊ������Һ��d��Ϊ��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ѡ��ҩƷ | ʵ������ | ����NaNO2������ |
| �ٷ�̪��Һ | ��Һ��� | ��Һ�Լ��� |
| �ڵ���-KI��ֽ | ��ֽ���� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 +ICl��
+ICl�� ��ICl�Ʊ�װ��ͼ��ͼ�����г�װ�ü�����������ʡ�ԣ���
��ICl�Ʊ�װ��ͼ��ͼ�����г�װ�ü�����������ʡ�ԣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 �����ܽ⡱��ͭԪ�ص���Ҫ������ʽ��Cu2+�������ӷ��ţ���
�����ܽ⡱��ͭԪ�ص���Ҫ������ʽ��Cu2+�������ӷ��ţ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ������ | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| ��ʼ����ʱ�� pH | 1.9 | 7.0 | 9.3 | 3.7 | 4.7 | �� |
| ������ȫʱ�� pH | 3.2 | 9.0 | 11.1 | 5.2 | 6.7 | 9����9�ܽ⣩ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com