
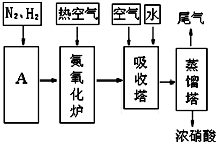
 CO+3H2��
CO+3H2������ ��1���ϳɰ��У������������ںϳ����з�Ӧ���ɰ�����������������Ϊ���Ӿ��壬����2С�����������Է��������ȡ�����ķ���Ϊ��Һ����������������������������Ϊ�������Դ���ȡ������ˮ�����ͼ��鷴Ӧ����һ����̼���������ݴ���д����ʽ��
��2������ƽ�ⳣ��������ʽ�����㣮
��� �⣺��1����ҵ�ϳɰ���ԭ����N2��H2���ϳɰ����豸�����У�ѹ�������ϳ�����������������������ѭ��ѹ������װ��AΪ�ϳ�����������Ϊѹ���ĵ�����������Ӧ���ɰ�������Ӧԭ��N2�ɴӿ����з���������������Ƚ�����Һ����Ȼ����������N2�ķе�������������������������ɵõ���ˮ�����ͼ��鷴Ӧ����һ����̼����������ӦΪ��CH4+H2O��g��  CO+3H2��
CO+3H2��
�ʴ�Ϊ���ϳ�����Һ������������N2�ķе����������CH4+H2O��g��  CO+3H2��
CO+3H2��
��2����CO����ʼŨ��Ϊxmol��H2O����ʼŨ��Ϊymol����ת����CO����СֵΪ0.8x��
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ x y 0 0
�仯 0.8x 0.8x 0.8x 0.8x
ƽ�� 0.2x y-0.8x 0.8x 0.8x��
����ƽ�ⳣ����ʽ��$\frac{��0.8x��^{2}}{0.2x����y-0.8x��}$=0.64��
��ã�$\frac{y}{x}$=5.8���ʴ�ֻҪ��ֵ����5.8��ת���ʾͻᳬ��80%��
�ʴ�Ϊ��5.8��
���� ���⿼��ѧ���ϳɰ���ԭ���Լ�Ӧ�õ�֪ʶ����һ����ѧ��������ϵ�Ŀ��⣬�漰���ʵķ��롢��ѧƽ��ĵ����⣬ע����������ʽ�������Ϊֱ�ۣ���Ŀ�Ѷ��еȣ�


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��AgCl����Һ�м���KI��Һ�����Ag++I-�TAgI�� | |
| B�� | NH4+��ˮ�ⷴӦ���ӷ���ʽ��NH4++H2O?NH3•H2O+H+ | |
| C�� | ��ͭʱ�������ĵ缫��ӦʽΪ��Cu2++2e-�TCu | |
| D�� | ij��Ӧ��H��0����÷�Ӧ�����������¾����Է����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
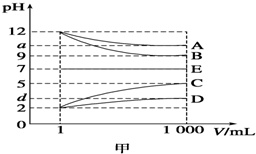 ����A��E�������±��е�������ɵģ������½������ʵ���Һ��1mLϡ�͵�1 000mL��pH�ı仯��ϵ��ͼ����ʾ������A��D��Ӧ�õ�E����ش��������⣮
����A��E�������±��е�������ɵģ������½������ʵ���Һ��1mLϡ�͵�1 000mL��pH�ı仯��ϵ��ͼ����ʾ������A��D��Ӧ�õ�E����ش��������⣮| ������ | NH4+��H+��Na+ |
| ������ | OH-��CH3COO-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | K1=1.76��10-5 | K1=4.9��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
| A�� | �к͵��������pH��CH3COOH��Һ��HCN��Һ����NaOH����ǰ�ߴ��ں��� | |
| B�� | �ɷ�����Ӧ��2CH3COOH+CO32-=2CH3COO-+H2O+CO2�� | |
| C�� | Na+��CN-��CH3COO-��HCO3-�������ܴ������� | |
| D�� | ��Ũ�ȵ�CH3COONa��NaCN��ҺpHǰ��С�ں��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
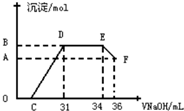 �о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�ͣ�ijͬѧȡһ���������Ͻ���һ������ϡ�������ַ�Ӧ����Ӧ������������ų�������Ӧ���������Һ�У���μ���2mol•L-1������������Һ����������������Һ�������mL��������ij��������ʵ�����mol���Ĺ�ϵ��ͼ��ʾ������ѡ����ȷ���ǣ�������
�о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�ͣ�ijͬѧȡһ���������Ͻ���һ������ϡ�������ַ�Ӧ����Ӧ������������ų�������Ӧ���������Һ�У���μ���2mol•L-1������������Һ����������������Һ�������mL��������ij��������ʵ�����mol���Ĺ�ϵ��ͼ��ʾ������ѡ����ȷ���ǣ�������| A�� | ͼ��OC�ε����ӷ���ʽΪ��NH4++OH-�TNH3•H2O | |
| B�� | ��DE�ε����ӷ���ʽΪ��H++OH-�TH2O | |
| C�� | B��A�IJ�ֵΪ 0.002mol | |
| D�� | C���Ӧ������������Һ�����Ϊ7 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��Ʒ��FeԪ�ص�����Ϊ2.24 g | B�� | ��ҺA�е�������ΪFe2+��Fe3+��H+ | ||
| C�� | ��Ʒ��CuO������Ϊ4.0 g | D�� | V=896 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu��OH��2��H2SO4 | B�� | Ba��OH��2��H2SO4 | C�� | Fe��OH��3��HCl | D�� | HNO3��KOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ32g O2 ��2NA��ԭ�� | |
| B�� | ��״����11.2L H2O ���е�ԭ����ĿΪ1.5NA | |
| C�� | 1mol��Cl- ����NA������ | |
| D�� | 0.5mol/L��NaCl ��Һ��Cl-�ĸ���Ϊ0.5 NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com