



 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������������һ�����ڷ�Ӧ�������� |
| B��ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
| C��һ�������£�0.5mol N2��1.5mol H2����ij�ܱ������г�ַ�Ӧ����NH3��������19.3kJ�����Ȼ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-38.6 kJ/mol |
D��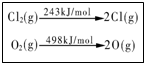 һ��������4 HCl��g��+O2��g��=2Cl2��g��+2H2O��g������1 molO2��Ӧ�ų�115.6 kJ������������ͼ��ʾ�������1 molH-O�������1 mol H-Cl������������Ϊ31.9 kJ һ��������4 HCl��g��+O2��g��=2Cl2��g��+2H2O��g������1 molO2��Ӧ�ų�115.6 kJ������������ͼ��ʾ�������1 molH-O�������1 mol H-Cl������������Ϊ31.9 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��һ�λ�ѧ�о���ѧϰʵ���У�ij�о�С��ѧ�����о�����ij��ƿ�ޱ�ǩ���Լ���ֻ֪��һƿ�ǹ��壬��һƿ��Һ�壬ȡ���������Լ����Թ��л�ϣ���������һ����ɫ��ζ�����壮������Դ����忪չһϵ��̽�������������ʵ�鱨�森
��һ�λ�ѧ�о���ѧϰʵ���У�ij�о�С��ѧ�����о�����ij��ƿ�ޱ�ǩ���Լ���ֻ֪��һƿ�ǹ��壬��һƿ��Һ�壬ȡ���������Լ����Թ��л�ϣ���������һ����ɫ��ζ�����壮������Դ����忪չһϵ��̽�������������ʵ�鱨�森| ���� | ʵ�鲽�� | ������ |
| ����������� | | __ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| SO | 2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com