
| A.浓硫酸 | B.碱石灰 | C.五氧化二磷 | D.固体NaOH |
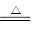 CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑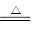 CaCl2+2H2O+2NH3↑。
CaCl2+2H2O+2NH3↑。

科目:高中化学 来源:不详 题型:单选题
| A.酸式滴定管不能装碱液,碱式滴定管不能装酸液或强氧化性溶液 |
| B.酸式滴定管用蒸馏水洗后,未用标准溶液润洗会引起测定结果偏高 |
| C.装待测液的锥形瓶应预先用待测液润洗 |
| D.在25.00 mL规格的滴定管中,当读数为15.00 mL时,实际体积大于10.00 mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 混合物 | 试剂 | 分离方法 |
| A | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
| B | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| D | 乙炔(硫化氢) | 硫酸铜 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
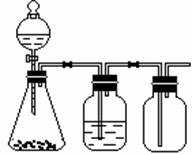
| 选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
| A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
| B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
| C | Zn 稀硫酸 | 浓硫酸 | H2 |
| D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向洗涤液中滴加碳酸钠溶液可检验沉淀是否洗涤干净 |
| B.上述变化过程中包括了分解、化合、复分解、置换等四种反应类型 |
| C.在氯化氢热气流中干燥晶体的目的是为了加快干燥速度 |
| D.步骤⑤也可以采用电解该盐水溶液的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
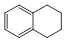
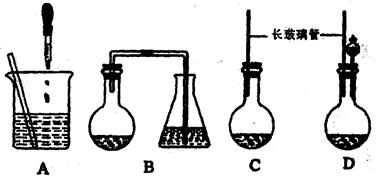
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.称取该晶体28.6 g溶于1 L水中 |
| B.称取10.6 g该晶体,溶于水制成1 L溶液 |
| C.将该晶体加热除去结晶水,称取10.6 g溶于水中制成1 L溶液 |
| D.称取该晶体28.6 g溶于水中制成1 L溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
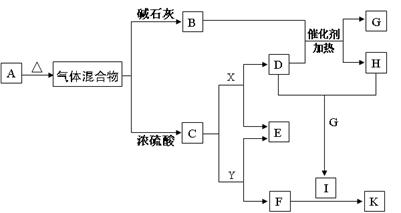
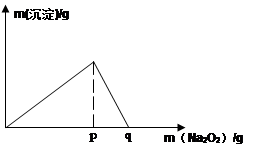
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com