
【题目】下列反应能用离子方程式CO![]() +2H+=CO2↑+H2O表示的是
+2H+=CO2↑+H2O表示的是
①Na2CO3+2HCl=2NaCl+CO2↑+H2O ②K2CO3+H2SO4=K2SO4+CO2↑+H2O
③CaCO3+2HCl=CaCl2+CO2↑+H2O ④2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O
A.①②B.①②③C.①③④D.②④
【答案】A
【解析】
①HCl是一元强酸,在溶液中完全电离,反应Na2CO3+2HCl=2NaCl+CO2↑+H2O的离子方程式为![]() +2H+=CO2↑+H2O,①符合题意;
+2H+=CO2↑+H2O,①符合题意;
②H2SO4是二元强酸,在溶液中完全电离,反应K2CO3+H2SO4=K2SO4+CO2↑+H2O的离子方程式为![]() +2H+=CO2↑+H2O,②符合题意;
+2H+=CO2↑+H2O,②符合题意;
③CaCO3难溶于水,不能拆写为离子形式,反应CaCO3+2HCl=CaCl2+CO2↑+H2O的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,③不符合题意;
④CH3COOH是一元弱酸,主要以分子形式存在,不能拆写为离子,所以2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O离子方程式为2CH3COOH+![]() =2CH3COO-+CO2↑+H2O,④不符合题意;
=2CH3COO-+CO2↑+H2O,④不符合题意;
答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.向Ba(AlO2)2溶液中加入过量NaHSO4溶液:Ba2++SO42-=BaSO4↓
B.泡沫灭火器中Al(SO4)3和NaHCO3溶液混合:Al3++3HCO3-=Al(OH)3↓+3CO2↑
C.以铜为电极,电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.向Cu(OH)2浊液中滴加饱和FeCl3溶液产生红褐色沉淀:Cu(OH)2+Fe3+Fe(OH)3+Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备直径为1-100nm的颗粒Y(化合物),反应原理为3Fe2++2![]() +O2+aOH-=Y+
+O2+aOH-=Y+![]() +2H2O,下列说法中不正确的
+2H2O,下列说法中不正确的
A.a=4
B.将Y均匀分散到水中形成的体系具有丁达尔效应
C.Fe2+、![]() 都是还原剂
都是还原剂
D.每有3molFe2+参加反应,反应中转移的电子总数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,2012年俄罗斯科学家再次合成117号元素。本次实验生成了6个新原子,其中5个![]() ,1个
,1个![]() 。下列关于
。下列关于![]() 和
和![]() 的说法不正确的是
的说法不正确的是
A. 是元素X的两种不同核素 B. 电子数相差1
C. 中子数分别为176和177 D. 它们互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池应用很广。某种锂离子二次电池的电极材料主要是钴酸锂(LiCoO2)和石墨。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大。
(1)锂离子电池(又称锂离子浓差电池)的工作原理:
ⅰ.充电过程:Li+从含LiCoO2的电极中脱出,正三价Co被氧化,此时该极处于贫锂态(Li1-xCoO2)。
ⅱ.放电过程原理示意图如图所示:
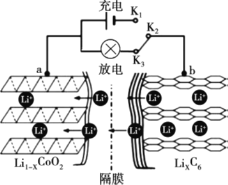
① 放电时,电子的流动方向为______。(用a、b、K2、K3)
② 放电时,正极的电极反应式为______。
(2)钴酸锂回收再生流程如下:
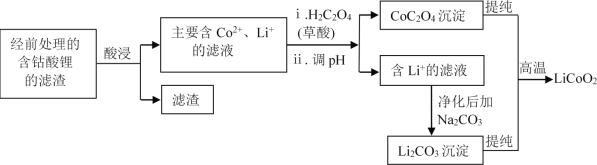
① 用H2SO4酸浸时,通常添加30%的H2O2以提高浸出效率,其中H2O2的作用是______。
② 用盐酸代替H2SO4和H2O2,浸出效率也很高,但工业上不使用盐酸。主要原因是:
ⅰ.会产生有毒、有污染的气体。写出相应反应的化学方程式_______。
ⅱ.Cl-对建筑材料的腐蚀及带来的水体问题等。
③ 其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30% H2O2 混合液中的浸出率曲线如图,请解释随着温度升高,钴的浸出率先升高后降低的原因:______。
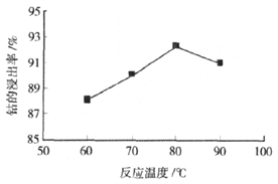
④ 已知草酸为二元弱酸,应用化学平衡移动原理,结合化学用语解释CoC2O4沉淀的同时溶液酸性增强的原因:______。
⑤ 高温下,在O2存在时纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组采用如下方案拆解废钴酸锂电池并从拆解的正极片中回收锂和钴,主要的实验流程如下:
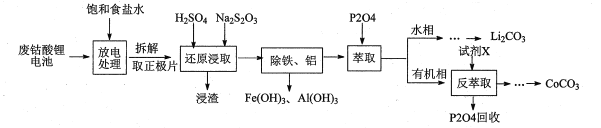
已知:①正极片中主要含LiCoO2(难溶于水)以及少量乙炔炭黑及铝箔等;负极为石墨,充电时Li+嵌入石墨电极。
②P2O4为磷酸二异辛酯,密度为0.973g.cm-3。
③3HBrO+CO(NH2)2=3HBr+N2↑+2H2O+CO2↑。
(1)“放电处理”时,有关说法正确的是__________(填标号)。
A.有利于锂的回收,提高锂的回收率
B.处理的主要目的是回收残余的电能
C.处理过程中产生的气体只有O2
D.可防止在电池拆解过程中,发生短路引起火灾、爆炸事故等安全问题
(2)“还原浸取”时,发生反应的离子方程式为_____________(S2O32-被氧化为SO42-)。
(3)“除铁、铝”时,应调整溶液的pH范围为___________(下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)。

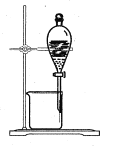
(4)“萃取”与“反萃取”时,静置后(如图所示),获得有机相的操作方法是__________;“反萃取”试剂X适宜是___________(填“H2SO4”或“NaOH”)溶液。
(5)设计以流程中产品Li2CO3为原料,制取LiBr·H2O的实验方案:向烧杯中加入适量冷水,______________,干燥得LiBr·H2O[实验中必须使用的试剂:饱和溴水、尿素及活性炭]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为ABC三套实验装置。
A、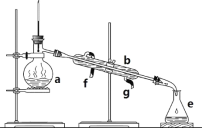 B、
B、 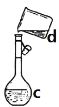 C、
C、 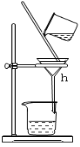
(1)写出下列仪器的名称:b.___, c._____,h.____。
(2)仪器a~e中,使用前必须检查是否漏水的有_____。(填序号)
(3)若利用装置分离酒精和水的混合物,还缺少的仪器是_____,将仪器补充完整后进行实验,冷凝水由____口流出(填f或g)。
(4)现需配制0.1mol/LNaOH溶液450mL,B装置是某同学转移溶液的示意图。
① B 图中的错误是_____。
② 根据计算得知,所需NaOH的质量为_______。
③ 配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
F.改用胶头滴管加水,使溶液凹面恰好与刻度相切
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作_______;容量瓶用蒸馏洗涤后残留有少量的水_________;若定容时俯视刻度线_______。
(6)将(4)所配溶液滴入盛有硫酸铜溶液试管中,可以观察到现象是_____,发生反应的离子方程式为_______,若将得到混合物进行分离,可选用分离方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。
(1)已知:CO2(g)+H2(g)![]() H2O(g) +CO(g) ΔH1 = + 41.1 kJmol-1
H2O(g) +CO(g) ΔH1 = + 41.1 kJmol-1
CO(g)+2H2(g)![]() CH3OH(g) ΔH2=-90.0 kJmol-1
CH3OH(g) ΔH2=-90.0 kJmol-1
写出CO2催化氢化合成甲醇的热化学方程式:_______。
(2)为提高CH3OH产率,理论上应采用的条件是_______(填字母)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),下图为不同投料比[n(H2)/n(CO2)]时某反应物X平衡转化率变化曲线。
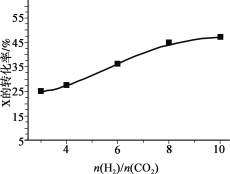
① 反应物X是_______(填“CO2”或“H2”)。
② 判断依据是_______。
(4)250℃、在体积为2.0L的恒容密闭容器中加入6mol H2、2mol CO2和催化剂,10min时反应达到平衡,测得c(CH3OH) = 0.75 mol· L-1。
① 前10min的平均反应速率v(H2)=_______ mol·L-1·min -1。
② 化学平衡常数K = _______。
③ 催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
实验编号 | 温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
D | span>553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
根据上表所给数据,用CO2生产甲醇的最优选项为_______(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.向CH3COOH中加入适量NaOH溶液:H++OH-=H2O
B.Fe与稀HNO3反应:Fe+2H+=Fe2++H2↑
C.Cl2通入H2O中:Cl2+H2O=2H++Cl-+ClO-
D.AlCl3溶液中加入过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com