
分析 (1)铁与过量的稀硝酸反应生成硝酸铁、一氧化氮和水,A可溶于C溶液中,则C为硝酸铁,D为NO;
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,为二氧化碳和二氧化硫,应是碳和浓硫酸能反应生成二氧化碳、二氧化硫和水;
(3)若C是无色刺激性气味的气体,其水溶液呈弱碱性,则C为氨气,应是氯化铵与氢氧化钙反应生成氨气、氯化钙与水.
解答 解:(1)(1)铁与过量的稀硝酸反应生成硝酸铁、一氧化氮和水,A可溶于C溶液中,则C为硝酸铁,D为NO,铁和铁离子能发生氧化还原反应生成亚铁离子,离子反应方程式为:2Fe3++Fe=3Fe2+,
故答案为:2Fe3++Fe=3Fe2+;
(2)若C、D均为气体,且都能使澄清石灰水变浑浊,而为二氧化碳和二氧化硫,碳和浓硫酸能发生氧化还原反应生成二氧化碳、二氧化硫和水,反应方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)若C是无色刺激性气味的气体,其水溶液呈弱碱性,则C为氨气,应是氯化铵与氢氧化钙反应生成氨气、氯化钙与水,反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2CaCl+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2CaCl+2NH3↑+2H2O.
点评 本题考查无机物推断,涉及Fe、硝酸、浓硫酸的性质及实验室氨气的制备,比较基础,注意基础知识的积累掌握.


科目:高中化学 来源: 题型:选择题
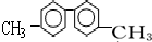
| A. | 该烃分子中有六种不同环境的氢原子 | |
| B. | 分子中至少有10个碳原子处于同一平面上 | |
| C. | 该烃的一氯代物最多有四种 | |
| D. | 该烃是苯的同系物,能使高锰酸钾和溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 央视焦点访谈节目在2010年10月报道,俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )
央视焦点访谈节目在2010年10月报道,俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )| A. | 该有机物的分子式为C7H10O3 | |
| B. | 1mol该有机物最多能与2mol H2发生加成反应 | |
| C. | 该有机物的一种芳香族同分异构体能发生银镜反应 | |
| D. | 该有机物能发生取代、加成、氧化和还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ).则1mol的该有机物跟足量的金属钠反应可以产生1.5molH2,1mol该有机物可以跟1molNaHCO3反应,1mol该有机物可以跟2molNaOH反应.
).则1mol的该有机物跟足量的金属钠反应可以产生1.5molH2,1mol该有机物可以跟1molNaHCO3反应,1mol该有机物可以跟2molNaOH反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol | B. | 2.8 mol | C. | 3.2 mol | D. | 3.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
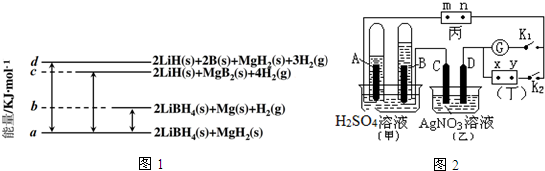
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | |||||||||||||||||
| f | h | i | |||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | k | ||||||||||||||
| l | |||||||||||||||||
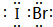 ,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.050 mol | B. | 0.060 mol | C. | 0.100 mol | D. | 0.200 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com