
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色。

(1)写出下列物质的化学式:A:____________;E:__________。
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:__________________。
(3)按要求写方程式:
B和R反应生成N的离子方程式:___________________________________;
M→W的离子方程式:_____________________________________________。
【答案】 Na2O2 FeCl2 生成白色沉淀,马上变成灰绿色,最终变成红褐色 2Al + 2OH- +2H2O = 2AlO2- + 3H2↑ Fe(OH)3+3H+=Fe3++3H2O
【解析】A为淡黄色固体,能与水反应,A是过氧化钠。C是无色无味的气体,C是氧气,B是氢氧化钠。T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,D是四氧化三铁,则T是铁,E是氯化亚铁,H是白色沉淀,H是氢氧化亚铁,M是氢氧化铁,W溶液中加入KSCN出现血红色,M是氯化铁。R是金属铝,N是偏铝酸钠,Q是氧化铝。
(1)根据以上分析可知A是Na2O2,E是FeCl2。(2)氢氧化钠溶液与氯化亚铁溶液反应生成氯化钠和氢氧化亚铁白色沉淀,氢氧化亚铁与氧气、水反应生成红褐色的氢氧化铁,可能观察到的现象:生成白色沉淀,马上变成灰绿色,最终变成红褐色。(3)B和R反应生成N的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑;M→W的离子方程式为Fe(OH)3+3H+=Fe3++3H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)![]() SO3(g)+NO(g) ,达到平衡,正反应速率随时间变化如图所示。则正确的结论是
SO3(g)+NO(g) ,达到平衡,正反应速率随时间变化如图所示。则正确的结论是
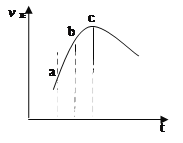
A. 逆反应速率:a点小于点c
B. 反应物浓度:a点小于点b
C. 反应在c点时处于平衡状态
D. 反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别表示生物体内的生物大分子的部分结构模式图,据图回答下列问题:

(1)图甲中的三种物质的基本单位都是___________,其中属于动物细胞储能物质的是___________。这三种物质中,在功能上与另外两种截然不同的是______________________。
(2)图乙化合物是肺炎双球菌遗传物质的一部分,其基本单位是__________,可用图中字母_______表示,各基本单位之间是通过___________(填①、②或③)连接起来的。
(3)图丙所示化合物的名称是___________,是由___________种氨基酸经___________过程形成的,脱去水中的氢元素来自___________,连接氨基酸之间的化学键是___________(填化学键结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得的浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示: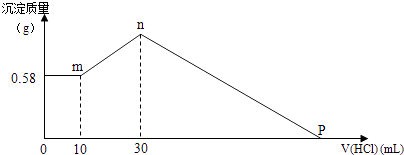
(1)混合物中NaOH的质量是g,AlCl3的质量是g.
(2)P点所表示盐酸加入体积为mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgCl2、Al2(SO4)3的混合溶液中不断加入NaOH溶液,得到沉淀的物质的量与加入NaOH溶液体积的关系如图所示,则原溶液中Mg2+与Al3+的物质的量之比是( )
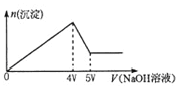
A. 1:2 B. 1:1 C. 2:3 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃科电池具有体积小,无需气体存储装置等优点。一种以胼(N2H4)为燃料的电池装置如下图装置①,该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列有关叙述不正确的是
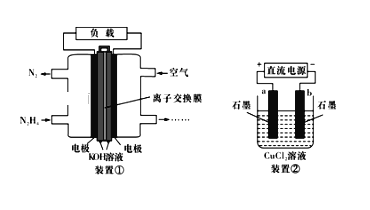
A. 该燃料电池负极发生的电极反应为:N2H4+4OH--4e-═N2↑+4H2O
B. 用该燃料电池作为装置②的直流电源,产生7.1gCl2至少需加入0.5molN2H4
C. 该燃料电池放电一段时间后,KOH溶液的pH保持不变(KOH溶液经充分搅拌且忽略反应过程中溶液体积的改变)
D. 该燃料电池的电极材料应采用多孔导电材料,其目的是提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化钡可用于制造电机电刷、光学玻璃、光导纤维、激光发生器。以钡矿粉(主要成分为BaCO3,含有SiO2、Fe2+、Mg2+等杂质)制备氟化钡的流程如下:
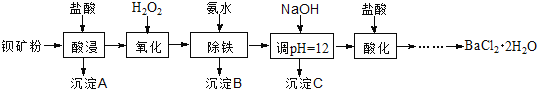
已知:常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。
(1)滤渣A的名称为___________。
(2)滤液1加H2O2的目的是___________。
(3)加NaOH溶液调节pH=12.5,得到滤渣C的主要成分是___________(写化学式)
(4)滤液3加入盐酸酸化后再经加热浓缩____________洗涤,真空干燥等一系列操作后得到BaCl2·2H2O晶体。
(5)常温下,用BaCl2·2H2O配制成0.2 mol/L水溶液与氟化铵溶液反应,可得到氟化钡沉淀。请写出该反应的离子方程式___________。已知Ksp(BaF2)=1.84×10-7,当钡离子完全沉淀时(即钡离子浓度≤10-5 mol/L),至少需要的氟离子浓度是___________mol/L(已知![]() =1.36,计算结果保留三位有效数字)。
=1.36,计算结果保留三位有效数字)。
(6)5.0 t含80%BaCO3的钡矿粉,理论上最多能生成BaCl2·2H2O晶体___________t 。(保留2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存且溶液颜色为无色的是( )
A.Na+、MnO4﹣、K+、NO3﹣SO32﹣
B.Na+、S2﹣、SO32﹣、H+、NO3﹣
C.Na+、S2﹣、OH﹣、K+、Cl﹣
D.HCO3﹣、H+、Na+、Ca2+SO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工集团为了提高资源利用率减少环境污染,将钛厂、氯碱厂和甲醇厂组成产业链.其主要工艺如下:
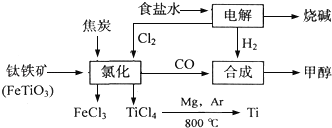
(1)写出电解食盐水反应的离子方程式________________________________。阳极上每生成标准状况下的11.2L气体,转移电子的物质的量是_______
(2)写出钛铁矿经氯化法得到四氯化钛的化学方程式:____________________。
(3)反应2Mg+TiCl4![]() 2MgCl4+Ti在Ar气氛中进行的理由是__________.
2MgCl4+Ti在Ar气氛中进行的理由是__________.
(4)在上述产业链中,合成192t甲醇理论上需额外补充H2_______t(不考虑生产过程中物质的任何损失)。
(5)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中负极上的电极反应式是___________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com