

图4-22
科目:高中化学 来源: 题型:
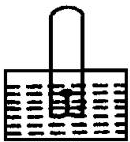 如图,水槽中试管内有一枚铁钉,放置数天观察.请回答下列问题:
如图,水槽中试管内有一枚铁钉,放置数天观察.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 人类的生活离不开化学,拥有化学知识可以使人类生活得更加自信.
人类的生活离不开化学,拥有化学知识可以使人类生活得更加自信.查看答案和解析>>
科目:高中化学 来源: 题型:
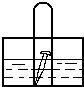 如图,水槽中试管内有一枚铁钉,放置数天观察:
如图,水槽中试管内有一枚铁钉,放置数天观察:查看答案和解析>>
科目:高中化学 来源: 题型:

(1)铁钉在逐渐生锈,则铁钉的腐蚀属于_____________腐蚀。
(2)若试管内液面上升,则原溶液是_____________性,发生_____________腐蚀,电极反应:负极_______________,正极_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com