
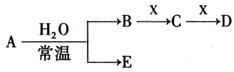
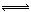 HCO3?+OH?
HCO3?+OH?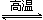 CO2+H2 50%
CO2+H2 50%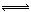 HCO3?+OH?
HCO3?+OH?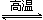 CO2+H2;设开始时CO和H2O的物质的量为1mol,转化的CO为x,则
CO2+H2;设开始时CO和H2O的物质的量为1mol,转化的CO为x,则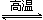 CO2+H2
CO2+H2

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.W的最高价氧化物对应的水化物是强酸 |
| B.Y的原子半径在同周期主族元素中最大 |
| C.W的非金属性比Z的弱 |
| D.Z的气态氢化物的稳定性在同主族元素中最强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
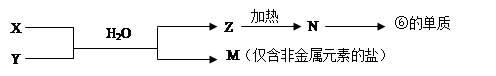
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
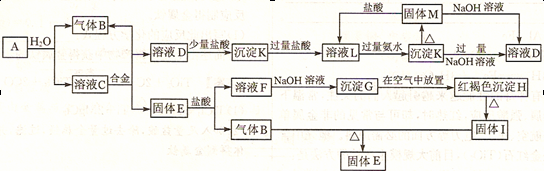
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
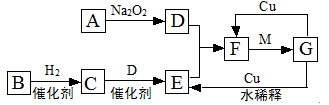
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钾与水的反应比钠与水的反应更剧烈 |
| B.溴单质与水的反应比氯单质与水的反应更剧烈 |
| C.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 |
| D.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
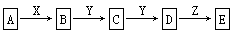
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com