某研究性学习小组在研究由Fe
2+制备Fe(OH)
2的过程中,设计了如下实验方案:
[实验设计]
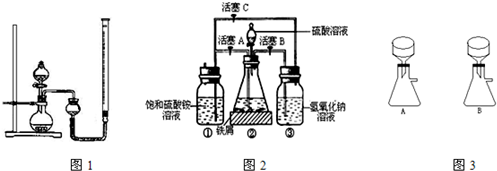
方法一:按照图1进行实验,容器A中的反应开始时,弹簧夹C处于打开状态,一段时间后,关闭弹簧夹C,容器A中的反应仍在进行.最终在
B
B
容器中观察到白色沉淀,该实验中涉及到的化学方程式有:
Fe+H2SO4=FeSO4+H2↑、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、H2SO4+2NaOH=Na2SO4+2H2O
Fe+H2SO4=FeSO4+H2↑、FeSO4+2NaOH=Fe(OH)2↓+Na2SO4、H2SO4+2NaOH=Na2SO4+2H2O
.
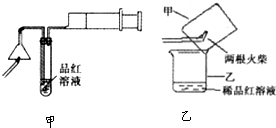
方法二:按图2进行实验,最终在两极间的溶液中首先观察到白色沉淀.请从所提供的试剂或电极材料中选择正确的序号填在横线上:
①纯水 ②NaCl溶液 ③NaOH溶液 ④四氯化碳 ⑤CuCl
2溶液 ⑥乙醇 ⑦Fe棒 ⑧植物油 ⑨碳棒
a为
⑦
⑦
,b为
⑨或⑦
⑨或⑦
,c为
⑧
⑧
,d为
②或③
②或③
.(填序号)
[探究思考]实验表明上述实验中出现白色的沉淀会逐渐转变为灰绿色或绿色,那么如何解释出现灰绿色或绿色的现象呢?
(1)甲同学查阅资料后,得到Fe(OH)
2如下信息:
| 资料名称 |
物理性质描述 |
化学性质描述 |
| 《化学辞典》,顾翼东编,1989年版P637 |
白色无定形粉末或白色至淡绿色六方晶体 |
与空气接触易被氧化,将细粉喷于空气中,则立即燃烧出火花 |
| 《大学普通化学(下册)》傅鹰著P637 |
白色沉淀 |
此沉淀易被氧化成微绿色Fe3(OH)8 |
| 《普通化学教程》(下册)P788 |
白色 |
能强烈吸收O2,迅速变成棕色Fe(OH)3.这时作为氧化的中间产物为土绿色,其中含有Fe2+、Fe3+. |
阅读该资料后,你对上述实验中出现灰绿色或绿色的现象的解释是:
由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3
由于Fe(OH)2部分被氧化,混入少量的Fe(OH)3
;资料中提及的微绿色Fe
3(OH)
8,用氧化物的形式表示可写成
FeO?Fe2O3?4H2O
FeO?Fe2O3?4H2O
.
(2)乙同学依据配色原理:白色和棕色不可能调配成绿色或灰绿色的常识,认为绿色可能是形成Fe(OH)
2?nH
2O所致.用热水浴的方式加热“方法一”中生成的绿色沉淀,观察到沉淀由绿变白的趋势.
加热时,“方法一”中弹簧夹C应处于
打开
打开
(填“打开”或“关闭”)状态,容器A中的反应须处于
发生
发生
(填“停止”或“发生”)状态.写出该实验中支持乙同学观点的化学方程式
.
(3)欢迎你参加该研究小组的讨论,请提出一种在研究由Fe
2+制备Fe(OH)
2的过程中,有助于对沉淀由“白”变“绿”的现象进行合理解释的实验设计新思路.
向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
向Fe2+和Fe3+的混合液中加入NaOH溶液后,观察生成的沉淀的颜色是否为灰绿色(或者可以将Fe(OH)3和Fe(OH)2混合后观察其颜色
.

 某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:
某研究性学习小组在研究由Fe2+制备Fe(OH)2的过程中,设计了如下实验方案:

 名校课堂系列答案
名校课堂系列答案