
����Ŀ����ҵ������������ʱ����ͬʱ������һ�ֳ�������Ҫ������������Ư����������(NaClO2)���乤���������£�
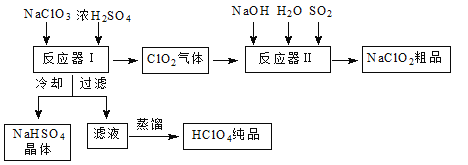
��֪����NaHSO4�ܽ�����¶ȵ����߶������ʵ������¿ɽᾧ������
�ڸ�����������Ϊֹ������֪���е���ǿ�ᣬ�е�90 ����
��ش��������⣺
��1����Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ ����ȴ��Ŀ���� ��������������������ԭ����___________________��
��2����Ӧ�����з�����Ӧ�����ӷ���ʽΪ__________________��
��3��ͨ�뷴Ӧ�����е�SO2��H2O2����ͬ��������NaClO2�����Ҫ˵��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ����_________________________��
��4��Ca(ClO)2��ClO2��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư��������Ϊ���Ƕ�����________________����д����ҵ����������NaOH��Һ����������NaClO�����ӷ���ʽ�� ��
���𰸡���1��3NaClO3+3H2SO4��HClO4+2ClO2��+3NaHSO4+H2O������NaHSO4���ܽ�ȣ�ʹNaHSO4�ᾧ������HClO4�е��
��2��2ClO2+SO2+4OH����2ClO2��+SO42��+2H2O
��3��H2O2�л�ԭ��Ҳ�ܰ�ClO2��ԭΪNaClO2
��4��ǿ��������Cl2+2OH����Cl��+ClO��+H2O
��������
�����������1�����������ѧ�������̷�����Ӧ������NaClO3��ŨH2SO4������Ӧ����HClO4��ClO2��NaHSO4��H2O����ѧ����ʽΪ3NaClO3 + 3H2SO4 �� HClO4 + 2ClO2�� + 3NaHSO4 + H2O����ȴ��Ŀ����������NaHSO4���ܽ����ʹNaHSO4�ᾧ������������������������ԭ���Ǹ�����ķе�͡�
��2����Ӧ������ClO2��SO2����������������Ӧ�����������ơ������ƺ�ˮ�����ӷ���ʽΪ2ClO2+SO2+4OH����2ClO2��+SO42��+2H2O��
��3��ͨ�뷴Ӧ�����е�SO2����һ����H2O2����ͬ��������NaClO2��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ����H2O2�л�ԭ��Ҳ�ܰ�ClO2��ԭΪNaClO2 ��
��4��Ca(ClO)2 ��ClO2��NaClO��NaClO2 �Ⱥ��Ȼ����ﶼ�dz��õ���������Ư������Ϊ���Ƕ�����ǿ����������������NaOH��Һ������һ��������NaClO�����ӷ���ʽΪCl2 + 2OH�� �� Cl�� + ClO�� + H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú����ȼú�糧�ķ�������Ҫ�ɷ�ΪSiO2��Al2O3��Fe2O3��C�ȡ�ʵ����ģ�ҵ�ӷ�ú����ȡ����Al2O3������������ͼ��

��֪�ս���̵IJ�����Ҫ�ǣ�NaAlO2��Ca2SiO4��NaFeO2��Na2SiO3�ȡ�
��1��д���ս��������Ԫ��ת���Ļ�ѧ����ʽ ��
��2������aΪ��ȴ����ĥ��������ĥ��Ŀ���� ��
��3�����������У�NaFeO2����ȫˮ�⣬ˮ�ⷴӦ�����ӷ���ʽΪ ��
��4������b�������� �����õIJ��������� �� ���ձ���
��5����̼����ʱ���ɳ����������Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��Һ���ܴ��������һ�������ǣ� ��
A��Pb2����Hg2����S2����SO42�� B��Na����Ba2����Cl����NO3��
C��H+��Na+��Fe2+��MnO4�� D��ClO����Al3����Br����CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��өʯ��������CaF2����������������ϵ���ڷ����Ƶľ�����ÿ��Ca2+��8��F������Χ����ÿ��F����Χ��������Ca2+��ĿΪ�� ��
A��2 B��4 C��6 D��8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��ͬѧ��4.48 L(������ɱ�״����)ij�л���������O2�г��ȼ�գ�Ȼ���ò�������ͨ��װ����ˮCuSO4�ĸ���ܡ�ʢ��ŨH2SO4��ϴ��ƿ��ʢ�к�0.8 mol Ca(OH)2�ij���ʯ��ˮ���ձ�����ͼ��ʾ��
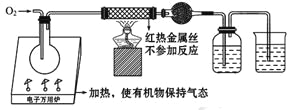
ʵ�����������ˮCuSO4����������ܺ�ϴ��ƿ������18 g������ʯ��ˮ����Ǻ���ǡ�ñ���塣�����ʵ��ش��������⣺
��1��O2Ҫ������ԭ���ǣ� ��______________________��______________________��
��2�������л���ֻ��C��H����Ԫ�أ��Ҳ����κι����ţ�Ҳ����֬��������л���ķ���ʽΪ_______������������_______(�����)��
A������ B������ͬϵ�� C�������� D������������
�����ʿ��ܵĽṹ��ʽΪ�� ��
��3�������л�������к���һ����ԭ�ӣ������������ļ������ʣ������һ������д���±��У�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NH2-������ͬ���������͵�����������( )
A. OH- B. NH4+ C. H3O+ D. CH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��Ħ������[��NH4��2Fe��SO4��2��6H2O]�Ƿ�����ѧ�е���Ҫ�Լ�����֪��Ħ���θ�������������500 ��ʱ����ȫ�ֽ⡣ijѧϰС����̽����ֽ���
��1����������롿С��ͬѧ��Ϊ�ֽ������������¼��������
A��Fe2O3 SO2 NH3 H2O
B��FeO SO3 NH3 H2O
C��FeO SO2 NH3 H2O
D��Fe2O3 SO3 SO2 NH3 H2O
������ѧ֪ʶ����ȷ��________�����������������
��2����ҩƷ�鴿����ͬѧ���������ʪ��ĺ�ɫʯ����ֽ��ϡ�����________��Һ�������Ħ���Ρ��е��������ӣ�ȡһ�����ġ�Ħ���Ρ������Һ��ȡ������Һ�����Թ��У������еμ�________�����Լ����ƺ�ʵ������������Ħ���Ρ�δ�����������ʡ�
��3����ʵ��̽����Ϊ����ֽ�����ͬѧ���������ʵ��װ�á�
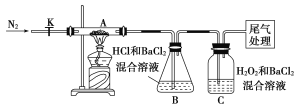
��ȡһ������Ħ���Ρ����ڼ��ȹ�A�У��������ֽ���ȫ���K����ͨ��N2��Ŀ����____________________��
��ʵ���й۲쵽A�й�����Ϊ����ɫ��B��C�о�������ɫ������C�з�����Ӧ�����ӷ���ʽΪ______________________��
��ʵ����֤��ȡA�в�������������ϡ�����ܽ⣬�ٵ���KMnO4ϡ��Һ������ɫ֤�����ﲻ��______________________��
��4����ʵ������뷴˼��ͨ��ʵ����������淴˼��������1��������һ����ȷ����________�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��DDT�ֽеε��飬��ѧ��Ϊ˫���ȱ����������飬��ѧʽ(ClC6H4)2CH(CCl3)�����ƴ�Ӣ����дDDT������Ϊ��ɫ���壬������ˮ������ú�ͣ����Ƴ����������Ч��ɱ�����DDT����ʳ�������ǵ���һЩʳ���ʳ�����ӽ��������Ҫԭ����˴�70�����ε�����������������ֹ������ʹ�á���ṹΪ��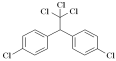 �������й�˵����ȷ���� ( )��ע������̼ԭ��Ϊ����̼ԭ��������4��ԭ�ӻ�ԭ���Ų�ͬ��
�������й�˵����ȷ���� ( )��ע������̼ԭ��Ϊ����̼ԭ��������4��ԭ�ӻ�ԭ���Ų�ͬ��
A����������
B��DDT��ȫȼ�պ�ֻ����CO2��H2O��������
C������������̼
D����˴Ź�����ͼ����5��λ�÷�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڹ����ŵ��ж���˵��������ǣ� ��
A�����Ĺ��������ǻ�����OH��
B������Ĺ��������ǻ�����OH��
C���ӵĹ��������ǻ�����OH��
D��ϩ���Ĺ�������̼̼˫��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com