
 的原子数目为NA.
的原子数目为NA. 分析 (1)等质量时,物质的分子个数与摩尔质量成反比;氧气和臭氧均由氧原子构成;
(2)同温同压下,气体摩尔体积相同,故等体积的气体的物质的量相等,而O2和O3所含的原子个数之比为2:3;当物质的量相等时,物质的质量之比等于摩尔质量之比;
(3)根据n=$\frac{m}{M}$计算水的物质的量,进而计算氢氧化钠的物质的量,根据m=nM计算氢氧化钠的质量;
(4)N2和CO的摩尔质量均为28g/mol,且氮气和CO均为双原子分子.
解答 解:(1)等质量时,物质的分子个数与摩尔质量成反比,故等质量的O2和O3的分子个数之比等于48:32=3:2;而氧气和臭氧均由氧原子构成,故等质量的氧气和臭氧中氧原子的个数相等,即1:1,故答案为:3:2;1:1;
(2)同温同压下,气体摩尔体积相同,故等体积的氧气和臭氧的物质的量相等,而O2和O3所含的原子个数之比为2:3,故等物质的量的氧气和臭氧中氧原子的个数之比为2:3;当物质的量相等时,物质的质量之比等于摩尔质量之比,故两者的质量之比为32:48=2:3,故答案为:2:3;2:3;
(3)90g 水的物质的量=$\frac{90g}{18g/mol}$=5mol,要使每10个水分子中溶有一个钠离子,则:n(NaOH)=$\frac{5mol}{10}$=0.5mol,故m(NaOH)=0.5mol×40g/mol=20g,
故答案为:20;
(4)N2和CO的摩尔质量均为28g/mol,故14g混合物的物质的量为0.5mol,而且氮气和CO均为双原子分子,故0.5mol混合气体中含1mol原子即NA个,故答案:NA.
点评 本题考查了物质的量和阿伏伽德罗常数的有关计算,熟练掌握公式的运用和物质的结构是解题的关键,难度不大.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:填空题
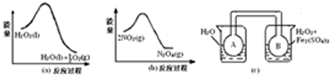
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 氢氟酸具有酸性 | 氢氟酸可用于雕刻玻璃 |
| B | 氯水显酸性 | 可用pH试纸测氯水的pH |
| C | NH3极易溶于水 | NH3可用作制冷剂 |
| D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂及操作 |
| A | 氢氧化钠 | 硫酸钠 | 加入适量氢氧化钙,过滤 |
| B | 生石灰 | 碳酸钙 | 高温锻烧 |
| C | 二氧化碳 | 一氧化碳 | 通过有足量灼烧氧化铁的玻璃管 |
| D | 氧化铜粉末 | 木炭粉 | 隔绝空气加强热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 | |
| B. | 人的皮肤在强紫外线的照射下将会失去生理活性 | |
| C. | 棉花和蚕丝的主要成分都是纤维素 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com