
�����14�֣�
����[ CaSx(x��5)]������������ɵĻ�����Ϊʯ��ϼ�������һ�ֺܺõ�ֲ��ɱ�����������Ǹ�ʯ�ҡ�ˮ�ȷ�Ӧ���á���ͬ��������Ǹ�ʯ����ˮ��Һ�з�Ӧ�������ɲ�ͬ�Ķ������������ơ�
3Ca(OH)2+8S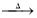 2CaS3+CaS2O3+3H2O��3Ca(OH)2+6S
2CaS3+CaS2O3+3H2O��3Ca(OH)2+6S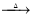 2CaS2+CaS2O3+3H2O
2CaS2+CaS2O3+3H2O
������м��㣺
52������ܽ���������Һ������һ�ֶ�����ö���������Ԫ�ص���������Ϊ0.736�����Na2Sx��x = ��
53��ȡijʯ��ϼ�������ֻ�����ֺ����250mL���ܶ�Ϊ1.12g/cm3��ͨ������CO2ʹ����ٷֽ⡣ԭ�����£� Sx2��+2H2O+2CO2��(x��1)S��+H2S��+2HCO3����S2O32��+ H2O+CO2��HSO3��+HCO3��+S����ȫ��Ӧ���ռ�������1.12������״������������������Һ�е��ܽ⣩�����ʯ��ϼ��ж��Ƶ����ʵ���Ũ��Ϊ ���������Ƶ���������Ϊ ��������С����ʾ������2λ��Ч���֣�
54���������ʯ�ҡ���Ǻ�ˮ��������7��16��70�������ȫ��Ӧ��ֻ�������ֺ���Ļ�������ʯ��ϼ��ж������������Ƶ����ʵ���֮���� �����ƵĻ�ѧʽ�� ��
55��������ʯ��50.4g�����96g��ˮ504gǡ����ȫ��Ӧ�������ֶ��ƣ�������CaS4֮��ж��ֶ��ơ�����������ֶ��ƿ��ܵ����ʵ���֮�ȣ�д���������̣���
����14�֣�52��4��2�֣���53��0.20 mol/L��2�֣��� 0.014��2�֣�
54��2��1��2�֣��� CaS5��2�֣���
55��n(CaS2)��n(CaS5)=1��2��2�֣���n(CaS3)��n(CaS5)=1��1��2�֣���
��������
���������52������ܽ���������Һ������һ�ֶ�����ö���������Ԫ�ص���������Ϊ0.736����Na2Sx �У�n(Na+)��n(Sx2-)=[(1-0.736)��23]��(0.736��32)=2:x�����x=4��
53��n(H2S)= 1.12L��22.4L/mol=0.05mol�����ж��Ƶ����ʵ�����0.05mol��c(CaSx)= 0.05mol��0.25L=0.20 mol/L ������2H2S+SO2=3S��+2H2O����n(CaS2O3)=1/2n(CaSx)= 0.025mol,�������Ƶ���������Ϊ(0.025mol��152g/mol)��(250mL��1.12g/cm3)=0.014��
54��m(CaO)��m(S)= 7��16����n(CaO)��n(S)= (7��56)��(16��32)=1:4.��CaO��ˮ��Ӧ������Ca(OH)2��S�����ʵ����ı���1:4.�ʷ�Ӧ�ķ���ʽ�ǣ�3Ca(OH)2+12S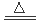 2CaSx+CaS2O3+3H2O�� x��5�����ƵĻ�ѧʽ��CaS5��n(CaSx)��n(CaS2O3)=2:1��
2CaSx+CaS2O3+3H2O�� x��5�����ƵĻ�ѧʽ��CaS5��n(CaSx)��n(CaS2O3)=2:1��
55��n(CaO)= 50.4g��56g/mol=0.3mol��n(S)= 96g��32g/mol=3mol����n(CaO)��n(S)=1:10����Ӧ����ʽ�ǣ�3Ca(OH)2+10S 2CaSx+CaS2O3+3H2O������Ԫ���غ�ɵ�x=4��������������ԭ�ӵ�ƽ��ֵΪ4����������ǡ����ȫ��Ӧ�������ֶ��ƣ�������CaS4֮��ж��ֶ��ơ������ֶ��������Ϊ��CaS2��CaS5��CaS3��CaS5 ������CaS2��CaS5��������ߵ����ʵ����ı���a:b����(2a+5b)/(a+b)=4���� a��b=1:2����n(CaS2)��n(CaS5)=1:2������CaS3��CaS5��������ߵ����ʵ����ı���m��n����(3m+5n) /(m+n)=4��m:n=1:1.��n(CaS3)��n(CaS5)=1:1��
2CaSx+CaS2O3+3H2O������Ԫ���غ�ɵ�x=4��������������ԭ�ӵ�ƽ��ֵΪ4����������ǡ����ȫ��Ӧ�������ֶ��ƣ�������CaS4֮��ж��ֶ��ơ������ֶ��������Ϊ��CaS2��CaS5��CaS3��CaS5 ������CaS2��CaS5��������ߵ����ʵ����ı���a:b����(2a+5b)/(a+b)=4���� a��b=1:2����n(CaS2)��n(CaS5)=1:2������CaS3��CaS5��������ߵ����ʵ����ı���m��n����(3m+5n) /(m+n)=4��m:n=1:1.��n(CaS3)��n(CaS5)=1:1��
���㣺����ʯ��ϼ�����ɡ��ṹ�����ʼ�Ӧ�õ�֪ʶ��


 С��ſ�ʱ��ҵϵ�д�
С��ſ�ʱ��ҵϵ�д� һ������ϵ�д�
һ������ϵ�д� �Ƹ�С״Ԫ���ֳ������ϵ�д�
�Ƹ�С״Ԫ���ֳ������ϵ�д� �¸��̵�ѧϵ�д�
�¸��̵�ѧϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�����Һ�У�����һ���ܴ����������
A��ǿ����Һ�У�Na+��Mg2+��SO42-��AlO2-
B��ij��ɫ��Һ�У�NH4+��Cu2+��MnO4-��NO3-
C������0.1 mol/L Fe3+��Һ�У�K+��Mg2+��Cl-��SCN-
D��������Ӧ����H2����Һ�У�Na+��K+��Cl-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ������
һ���¶��£����ݻ�Ϊ2 L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯��ͼ��ʾ��

��ش��������⣺
��1��д���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2��0-6 s�ڣ�B��ƽ����Ӧ����Ϊ�� ��
��3������˵����ȷ���ǣ� ��
A����Ӧ���е�1 sʱ��v��A����v��D��
B����Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
C����Ӧ���е�6 sʱ��Ӧֹͣ��
D������Ӧ�ﵽƽ��״̬ʱ4v(A)=5v(C)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и߶���ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ȷ�Ӧ�����ȷ�Ӧ�������У���ȷ����
�������Ӧ�����������������������������÷�Ӧһ�������ȷ�Ӧ��
��ֻҪ���ڼ��������½��еķ�Ӧ��һ�������ȷ�Ӧ
��ֻҪ���ڳ��³�ѹ�½��еķ�Ӧ��һ���Ƿ��ȷ�Ӧ
���кͷ�Ӧ��ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ
�ݻ��Ϸ�Ӧ���Ƿ��ȷ�Ӧ
��ԭ��ط�Ӧ�����Ƿ��ȷ�Ӧ��Ҳ���������ȷ�Ӧ
A���� �� B���� �� �� C���� �� �� D���� �� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��ɽ�и�����һ�ε����о��������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ס��ҡ�����X����ѧ��ѧ�г�����4�����ʣ���ת����ϵ����ͼ��
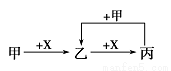
���м�X��������
A����ΪFe��XΪCl2
B����ΪSO2��XΪNaOH��Һ
C����ΪC��XΪO2
D����ΪAlCl3��Һ��XΪNaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ�����У������ѧ�����Ͻ�ѧ�������л�ѧ�Ծ��������棩 ���ͣ������
������14�֣�
�ϳɰ��������ѧ�����ϵ�һ���ش�ͻ�ƣ��䷴Ӧԭ��Ϊ�� N2(g)+3H2(g)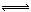 2NH3(g)+Q��Q��0��
2NH3(g)+Q��Q��0��
һ�ֹ�ҵ�ϳɰ��ļ�������ͼ���£�
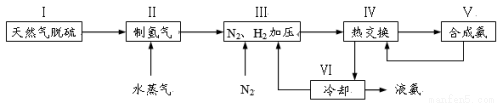
���������գ�
28����Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������NH4HS�ĵ���ʽ��_______________��д��������Ӧ�Ļ�ѧ����ʽ��_______________��NH3�ķе����H2S������ΪNH3����֮�������һ�ֱ�_________����ǿ����������
29�������£�0.1 mol/L���Ȼ����Һ��0.1 mol/L�����������Һ�����Ը�ǿ����_______����ԭ����_______��
��֪��H2SO4��Ki2=1.2��10��2 NH3��H2O��Ki=1.8��10��5
30��ͼ�ױ�ʾ500�桢60.0MPa�����£�ԭ����Ͷ�ϱ���ƽ��ʱNH3��������Ĺ�ϵ������ͼ��a�����ݼ���N2��ƽ�����������______������С����ʾ������3λ��Ч���֣���
31�������¶ȶԺϳɰ���Ӧ��Ӱ�죬��ͼ������ϵ�У�����һ�������µ��ܱ������ڣ���ͨ��ԭ������ʼ�����¶Ȳ������ߣ�NH3���ʵ����仯������ʾ��ͼ��


32����������ͼ�У�ʹ�ϳɰ��ų��������õ�������õ���Ҫ�����ǣ�����ţ�________��
��������������ߺϳɰ�ԭ����ת���ʵķ�����________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ϻ�����У������ѧ�����Ͻ�ѧ�������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ʯīΪ�缫����⺬��������̪�͵��۵�NaI��Һ����֪��ͨ�������£�I���ķŵ�������Cl����ǿ������˵���������
A������������Һ�ʺ�ɫ B�������ݳ�����
C������������Һ����ɫ D����Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڽ��Ŀ��Ի�ѧ�Ծ��������棩 ���ͣ�������
��ͭ����Ҫ�ɷ�CuFeS2������ȡͭ����Ҫԭ��
��֪��2CuFeS2��4O2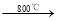 Cu2S��3SO2��2FeO?¯������Cu2S��1200������¼�����Ӧ�� 2Cu2S��3O2 �� 2Cu2O��2SO2�� 2Cu2O��Cu2S �� 6Cu��SO2���ٶ�������Ӧ����ȫ��������м��㣺
Cu2S��3SO2��2FeO?¯������Cu2S��1200������¼�����Ӧ�� 2Cu2S��3O2 �� 2Cu2O��2SO2�� 2Cu2O��Cu2S �� 6Cu��SO2���ٶ�������Ӧ����ȫ��������м��㣺
����6 mol CuFeS2����6 mol Cu��������O2�����ʵ��� mol
�� 6 mol CuFeS2��14.25 mol O2��Ӧ�������Ͽɵõ� molͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��amol��Na2O2��bmol��NaHCO3�����Ϻ����ܱ������м��ȵ�250�棬�����ַ�Ӧ������˵���������
A����ʣ�����ΪNa2CO3���ų�����ΪO2��H2Oʱ��a:b=1:2
B����ʣ�����ΪNa2CO3,NaOH���ų�����ΪO2��H2Oʱ 1/2<a:b<1
C����a:b>1ʱ��ʣ�����ΪNa2O2,Na2CO3,NaOH���ų�����ΪO2
D�����ų���O2��H2OΪ�����ʵ���ʱ����a:b=3:2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com