
| A、m>n | B、m<n |
| C、m=n | D、不能确定 |
| n |
| V |


科目:高中化学 来源: 题型:
| A、金属钠溶于水:Na+2H2O═Na++2OH-+H2↑ |
| B、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| C、碳酸钙与盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、硫酸铝溶液与氨水的反应:Al3++3OH-═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应开始4 min内温度对反应速率的影响比浓度大 |
| B、一段时间后,反应速率减小的原因是c(H+)减小 |
| C、反应在2~4 min内平均反应速率最大 |
| D、反应在2~4 min内生成CO2的平均反应速率为V(CO2)=0.1 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
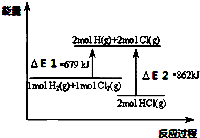
| A、△E1是该反应的活化能 |
| B、△E2是破坏2mol HCl(g)所需的能量 |
| C、该反应的热化学方程式为:H2+Cl2=2 HCl△H=-183KJ/mol |
| D、该反应是一个反应物总能量高于生成物总能量的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 )是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖.
)是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1×10-4mol/L |
| B、1×10-10mol/L |
| C、(1×10-4-1×10-10)mol/L |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1<T2 |
| C、反应Ⅲ:△H<0,T2>T1 |
| D、反应Ⅳ:△H>0,T2>T1;或△H<0,T2<T1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com