
下列实验事实与平衡移动无关的是( )
|
| A. | 氯气难溶于饱和食盐水 |
|
| B. | 用加压的方法促进CO2在水中的溶解 |
|
| C. | FeCl3+3KSCN⇌Fe(SCN)3+KCl,向体系中加入KCl固体 |
|
| D. | 合成氨工业中,及时将氨气液化移出 |
考点:
化学平衡移动原理.
专题:
化学平衡专题.
分析:
平衡移动原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.平衡移动原理适用的对象是可逆过程,如与可逆过程无关,则不能用平衡移动原理解释,平衡移动原理对所有的动态平衡都适用.
解答:
解:A.氯气和水反应生成盐酸和次氯酸,该反应存在溶解平衡,饱和食盐水中含有氯化钠电离出的氯离子,抑制了氯气的溶解,所以用排饱和食盐水的方法收集氯气,可以用平衡移动原理来解释,故A错误;
B、加压能使CO2在水中的溶解向着溶解的方向进行,与平衡移动有关,故B错误;
C、平衡体系固体物质量的增减不会对化学平衡的移动产生影响,与平衡移动无关,故C正确;
D、合成氨工业中,及时将氨气液化移出,可以促进合成氨的反应平衡正向移动,与平衡移动有关,故D错误;
故选C.
点评:
本题考查了平衡移动原理的使用对象,难度不大,注意使用平衡移动原理的前提必须是可逆反应,细心体会化学平衡移动原理是很重要的.


科目:高中化学 来源: 题型:
将标准状况下的a L HCl(g)溶于1000g水中,得
到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是( )
A.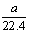 mo1·L-1 B.
mo1·L-1 B.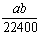 mol·L-1 C.
mol·L-1 C.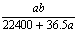 mol·L-1 D.
mol·L-1 D.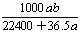 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列组合中,属于含有极性键的非极性分子的是( )
|
| A. | C2H4、C2H2、CO2 | B. | CH4、CHCl3、CO2 |
|
| C. | Cl2、H2、N2 | D. | NH3、H2O、SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
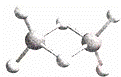
近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧时放出大量的热量.Al2H6球棍模型如图.下列说法肯定错误的是( )
|
| A. | Al2H6在固态时所形成的晶体是分子晶体 |
|
| B. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 |
|
| C. | Al2H6在空气中完全燃烧,产物为氧化铝和水 |
|
| D. | Al2H6中含有离子键和极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,将等物质的量的P与Q投入体积固定2L密闭容器中,发生反应2P(g)+Qg)⇌xW(g)+U(g),经5min后到达平衡,这5min内W的平均反应速率是0.2mol/(L•min),平衡时U的浓度为0.5mol/L,[P]:[Q]=1:2,下列说法中不正确的是( )
|
| A. | x值是2 |
|
| B. | P平衡转化率为66.7% |
|
| C. | 平衡常数为1 |
|
| D. | 反应前,Q的物质的量为3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液电导率与溶液中各离子的总浓度有关,离子浓度越大,溶液电导率越大.现在向甲溶液中加入等浓度的乙溶液至恰好反应,混合溶液电导率与乙溶液体积的关系曲线如下所示,其中曲线错误的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
能够鉴定氯乙烷中氯元素的存在的最佳操作是( )
A. 在氯乙烷中直接加入AgNO3溶液
B. 加蒸馏水,充分搅拌后,加入AgNO3溶液
C. 加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
D. 加入NaOH的乙醇溶液,加热后加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个密闭容器中用等物质的量的A和B发生反应:A(g)+3B(g) 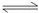 2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )
2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )
|
| A. | 50% | B. | 60% | C. | 70% | D. | 无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com