
【题目】现有下列物质:
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 CH3CH2OH MgO MgCl2 KOH HCl Al2O3
请回答下列问题。
(1)两性氧化物是___(填序号),其电子式为___。
(2)最简单的有机化合物是___(填序号),用电子式表示其形成过程:___。
(3)属于共价化合物的是___(填序号),含有共价键的离子化合物是___(填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___(填序号),这两种元素的单质反应生成该化合物的化学方程式为___。
【答案】 ![]() ②
② 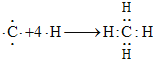 ②⑥⑧⑨ ③⑤ ⑤ 2Na+O2
②⑥⑧⑨ ③⑤ ⑤ 2Na+O2![]() Na2O2
Na2O2
【解析】
(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物;
(2)最简单的有机化合物是CH4,甲烷为共价化合物;
(3) 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物;
(4)由两种元素组成,且离子键、共价键都含有的是Na2O2。
(1)两性氧化物指的是能与碱和酸反应生成盐和水的氧化物,这里只有Al2O3,Al2O3是离子化合物,其电子式为:![]() ,故答案为:;
,故答案为:;![]() ;
;
(2)最简单的有机化合物是CH4,甲烷为共价化合物,用电子式表示其形成过程为: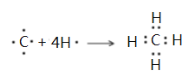 ,故答案为:②;
,故答案为:②;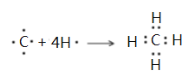 ;
;
(3)只含共价键的化合物为共价化合物,CH4、HClO4、CO、SO2、CH3CH2OH、HCl中只含共价键,属于共价化合物;含有共价键的离子化合物有:NH4NO3、Na2O2、KOH,故答案为:②⑥⑧⑨ ;③⑤ ;
(4)由两种元素组成,且离子键、共价键都含有的是Na2O2,钠和氧气反应生成过氧化钠的化学方程式:2Na+O2![]() Na2O2,故答案为:⑤;2Na+O2
Na2O2,故答案为:⑤;2Na+O2![]() Na2O2。
Na2O2。


科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式书写正确的是
A.FeCl3溶液刻蚀铜电路板:Fe3++Cu=Cu2++Fe2+
B.用小苏打治疗胃酸过多:HCO3-+H+= CO2↑+H2O
C.将饱和FeCl3溶液滴入沸水制得Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
D.向Ba(OH)2溶液中滴加NaHSO4溶液使Ba2+刚好沉淀完全:Ba2++2OH-+SO42-+2H+=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国家实施“青山绿水工程”,大力研究脱硝和脱硫技术。
(1)H2在催化剂作用下可将NO还原为N2。下图是该反应生成1 mol水蒸气的能量变化示意图。写出该反应的热化学方程式____________(△H可用E1、E2、E3表示)。

(2)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓

①装置中H+向________池迁移。
②乙池溶液中发生反应的离子方程式:____________
(3)2NO(g)+O2(g)![]() 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
反应I:2NO(g)![]() N2O2(g)(快);
N2O2(g)(快);![]() <0 v1正=k1正 c2(NO) 、v1逆=k1逆 c(N2O2)
<0 v1正=k1正 c2(NO) 、v1逆=k1逆 c(N2O2)
反应Ⅱ:N2O2(g)+O2(g)![]() 2NO2(g)(慢)
2NO2(g)(慢) ![]() 2<0 v2正=k2正 c(N2O2)c(O2) v2逆=k2逆 c2(NO2);
2<0 v2正=k2正 c(N2O2)c(O2) v2逆=k2逆 c2(NO2);
在一定条件下,反应2NO(g)+O2(g)![]() 2NO2(g)达到平衡状态,平衡常数=___________(用含K1正、K1逆、K2正、K2逆的代数式表示)。
2NO2(g)达到平衡状态,平衡常数=___________(用含K1正、K1逆、K2正、K2逆的代数式表示)。
(4)废水处理时,通H2S(或加S2-)能使某些金属离子生成极难溶的硫化物而除去。25°℃,某废液中c(Mn2+)=0.02mol·L-1,调节废液的pH使Mn2+开始沉淀为MnS时,废液中c(H2S)=0.1mol·L-1,此时pH约为____。(已知:Ksp(MnS)=5.0×10-14,H2S的电离常数:K1=1.5×10-7,K2=6.0×10-15,1g6=0.8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如下实验探究铁钉在不同溶液中的吸氧腐蚀。下列说法不正确的是
实验装置 | 实验编号 | 浸泡液 | pH | 氧气浓度随时间的变化 |
|
|
| 5 |
|
|
| 5 | ||
|
| 7 | ||
|
| 7 |
A.上述正极反应均为![]()
B.在不同溶液中,![]() 是影响吸氧腐蚀速率的主要因素
是影响吸氧腐蚀速率的主要因素
C.向实验![]() 中加入少量
中加入少量![]() 固体,吸氧腐蚀速率加快
固体,吸氧腐蚀速率加快
D.![]() 内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液
内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A. ①②③⑤ B. ③⑥ C. ③ D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20mL0.1000mol·L-1氨水用0.1000mol·L-1的盐酸滴定,滴定曲线如图,下列说法正确的是( )
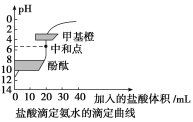
A.该中和滴定适宜用酚酞作指示剂
B.两者恰好中和时,溶液的pH=7
C.达到滴定终点时,溶液中:c(H+)=c(OH-)+c(NH3·H2O)
D.当滴入盐酸达30 mL时,溶液中c(NH4+)+c(H+)<c(OH-)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.已知0.1 mol·L-1的CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液
CH3COO-+H+,加少量烧碱溶液可使溶液 增大
增大
B.25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O![]() H++OH-逆向移动,c(H+)降低
H++OH-逆向移动,c(H+)降低
C.室温下向10 mL pH=3的醋酸溶液中加水稀释后,溶液中![]() 不变
不变
D.0.1 mol·L-1的醋酸加水稀释后,溶液中所有离子的浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)写出H2CO3电离方程式_________平衡常数表达式Ka1(H2CO3)=__________________
(2)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________
(3)①CH3COO-、②HCO3-、③CO32-、④ClO-结合H+的能力由强到弱的顺序为(注意:用序号①、②、③、④作答)____________________
(4)体积为10mLpH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数__________(填“大于”、“等于”或“小于”)醋酸的平衡常数。
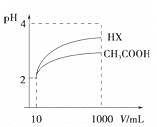
(5)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化为放热反应的是( )
A.H2O(g)=H2O(l) △H=-44.0 kJ/mol
B.2HI(g)=H2(g)+I2(g) △H=+14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如图所示的化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com