
| A. | 从1L1mol/L的氯化钠溶液中取出10ml后,其浓度仍是1mol/L | |
| B. | NaHSO4溶液与NaOH溶液反应的离子方程式:H++OH-=H2O | |
| C. | FeCl3溶液呈电中性,Fe(OH)3胶体带正电 | |
| D. | 氧化剂具有氧化性,是得到电子(或电子对偏向)的物质,反应时本身被还原 |
分析 A.溶液的物质的量浓度不随溶液体积的变化而变化;
B.NaHSO4溶液与NaOH溶液反应生成硫酸钠和水;
C.Fe(OH)3胶体能吸附正电荷;
D.所含有元素的化合价降低得电子的物质为氧化剂.
解答 解:A.溶液的物质的量浓度不随溶液体积的变化而变化,所以从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L,故A正确;
B.NaHSO4溶液与NaOH溶液反应生成硫酸钠和水,NaHSO4、NaOH、硫酸钠均为易溶于水的强电解质,要改写成离子,其离子方程式为:H++OH-=H2O,故B正确;
C.Fe(OH)3胶体不带电荷,但是Fe(OH)3胶体粒子能吸附正电荷,故C错误;
D.所含有元素的化合价降低得电子的物质为氧化剂,氧化剂在反应中被还原,故D正确.
故选C.
点评 本题考查氧化还原反应,题目难度不大,注意把握元素化合价的判断,从化合价变化的角度分析,题目侧重于相关概念的考查.


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Fe3+、NO3-、SO42-、Na+ | |
| B. | 使酚酞变红色的溶液中:Na+、Al3+、HCO3-、NO3- | |
| C. | 能与金属铝反应生成氢气的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 无色透明的溶液中:K+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | B电极发生还原反应 | |
| B. | A电极上发生的一个电极反应为:2Li++S8+2e-═Li2S8 | |
| C. | 每生成1mol Li2S8转移0.25mol电子 | |
| D. | 电子从B电极经过外电路流向A电极,再经过电解质流回B电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2在大气中能最终生成H2SO4:2SO2+O2+2H2O═4H++2SO42- | |
| B. | 少量SO2与NaOH溶液反应的离子方程式是:SO2+OH-═HSO3- | |
| C. | NaOH溶液缓慢吸收过量SO2的过程中有:SO2+SO32-+H2O═2HSO3- | |
| D. | n(SO2):n(NaOH)=1:2时,溶液pH>7:SO32-+H2O?HSO3-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
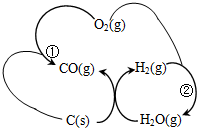 燃煤厂为减少SO2的排放,可采取的措施是:
燃煤厂为减少SO2的排放,可采取的措施是:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 40% | B. | 50% | C. | 80% | D. | 90% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物总能量一定低于反应物总能量 | |
| B. | △H的大小与热化学方程式的计量系数无关 | |
| C. | 应用盖斯定律可计算某些难以直接测量的反应烩变 | |
| D. | 同温同压下,H2(g)十Cl2(g)=2HC1(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 1mol分子中的化学键断时需要吸收能量/kJ | H2(g) | Cl2(g) | HCl(g) |
| 436 | 243 | 431 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com