
| A、①③ | B、②④ | C、②⑤ | D、④⑥ |


科目:高中化学 来源: 题型:
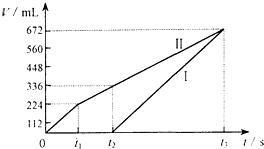 常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:
常温下电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如图Ⅰ、Ⅱ所示(气体体积已换算成标准状况下的体积),根据图中信息进行下列计算:查看答案和解析>>
科目:高中化学 来源: 题型:
| 被提纯的物质 [括号内物质是杂质] | 除杂试剂 | 除杂方法 | |
| A | CO(g)[CO2(g)] | NaOH溶液、浓H2SO4 | 洗气 |
| B | NH4Cl(aq)[Fe3+(aq)] | NaOH溶液 | 过滤 |
| C | Cl2(g)[HCl(g)] | 饱和食盐水、浓H2SO4 | 洗气 |
| D | Na2CO3(s)[NaHCO3(s)] | - | 加热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
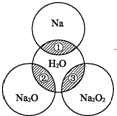 如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、Na2O2晶体中阴阳离子数目之比为1:1 |
| B、反应③最多能产生0.05 mol O2 |
| C、反应①的离子方程式为Na+2H2O═Na++2OH-+H2↑ |
| D、①、②、③充分反应后所得溶液的质量分数从大到小的顺序为①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当溶液中Al3+全部沉淀出来时,沉淀的总物质的量最大 |
| B、当溶液中Al3+全部沉淀出来时,沉淀的总质量最大 |
| C、先生成沉淀,后沉淀全部溶解 |
| D、最后的沉淀为2mol BaSO4、1mol Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+、NO3-、Al3+、Cl- |
| B、Na+、SO32-、K+、Cl- |
| C、MnO4-、K+、SO42-、Na+ |
| D、K+、SO42-、HCO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 所含离子 | NO3- | SO42- | H+ | M |
| 浓度/(mol?L-1) | 2 | 1 | 2 | 1 |
| A、Na+ |
| B、Ba2+ |
| C、F- |
| D、S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com