
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)![]() 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是( )
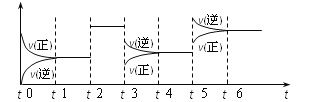
A. t5时增大了压强 B. t3时降低了温度
C. t2时加入了催化剂 D. t4~t5时间内转化率一定最低
科目:高中化学 来源: 题型:
【题目】滴定法是化学常用来定量测定物质浓度的一种重要的实验方法。在食品工业、药品制造、化妆品行业等等都被广泛应用。中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用如图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
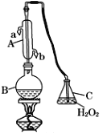
(1)仪器A的名称是________,水通入A的进口为________。B中加入300.00 mL葡萄酒和适量盐酸,加热B使SO2全部逸出并与C中H2O2完全反应。
(2)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,若滴定终点时溶液的pH=8.8,则选择的指示剂为________。滴定终点现象为_______________。
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为:________g·L-1。
(4)该测定结果往往比实际值偏高,最可能的原因是_________________,在不改变装置的情况下,如何改进:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Na+、Al3+、Fe2+、Fe3+、Cu2+、Ag+、CO32-、S2-、SO32-、AlO2-、Cl-、SO42-中的一种或几种,对该溶液进行实验,结果如图:

下列说法不正确的是( )
A. 淡黄色沉淀甲为AgBr,沉淀乙为Al(OH)3
B. 溶液中一定含有Na+、S2-、SO32-、AlO2-
C. 气体甲的成分可能是CO2或SO2或H2S或CO2、SO2的混合气体或CO2、H2S的混合气体
D. 确定溶液A中是否含有SO42-,可在沉淀丙中加入足量稀盐酸,若沉淀部分溶解则溶液A中含有SO42-,若沉淀全部溶解则溶液A中不含SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知a、b、c、d四种元素均为短周期主族元素,原子序数依次递增,c元素的单质或含c元素的化合物,焰色反应显黄色,a、b两原子可形成常温下呈液态的的X、Y两种化合物,其中X中a与b原子个数之比为2:1,Y中a与b原子个数之比为1:1,若用a、b、c、d表示它们的单质,单质之间有如下反应:

化合物之间反应:甲+Z→X + d;甲+Y →M。
M常温下是油状液体,它的浓溶液在常温下可用铁或铝制器运输保存。它的浓溶液和另一种酸的浓溶液常用来制炸药,M也用来制磷酸,M还可用于制铅蓄电池。
(1)写出C的元素符号: _________ ,Y的电子式:_______________;
(2)在30%的Y的水溶液中加入MnO2,有大量b的单质气体放出,若在Y、MnO2的混合液中加入稀H2SO4,MnO2被还原成Mn2+ ,仍然产生大量b的单质气体,写出其离子方程式___________________________;
(3)向盛有NaOH和Y的混合液的烧杯中缓缓导入Cl2,产生火光和爆炸声,其中NaOH的作用是_________,对应离子方程式 ____________________________;
(4)由b、c、d三种元素可形成中学化学常见的三种盐丙、丁、戊,其相对分子质量依次增大。戊+M→丁+甲↑+d↓+X,在戊的水溶液中导入甲气体也有d单质的淡黄色沉淀。写出戊和M在水溶液中化学方程式___;
(5)由和M具有相同元素组成的化合物A的分子式为a2d2b8.工业上电解50%的M的水溶液可制得A,发生的反应为:2M![]() A+a2↑,写出阳极电极反应方程式:__________;将A溶液进行稀释又可制得Y。
A+a2↑,写出阳极电极反应方程式:__________;将A溶液进行稀释又可制得Y。
(6)利用c、d两单质之间的反应,可设计一种原电池反应:2C+d![]() C2d,其中正极的电极反应式为:____。
C2d,其中正极的电极反应式为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如下图所示。下列说法正确的是
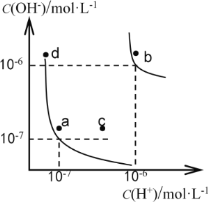
A. 图中对应点的温度关系为: a>b
B. 水的电离常数KW数值大小关系为:b>d
C. 温度不变,加入少量NaOH可使溶液从c点变到a点
D. 在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】置换反应可表示为

下列说法不正确的是
A. 若A、B都是短周期元素,则B的原子序数可能是A的两倍
B. 若乙是一种常见的半导体材料,则通过该反应说明A的非金属性一定比B强
C. 若A、B均为非金属元素,则该反应过程中可能会产生白烟
D. 该反应可用于某些金属的冶炼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Hln在水溶液中存在电离平衡:HIn(红色)H++In-(黄色),故可用做酸碱指示剂。下列稀溶液中能使指示剂由黄色变为红色的是
A.盐酸B.氢氧化钠溶液C.食盐溶液D.氨水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com