
| A、硫酸,纯碱,氯化钠 |
| B、硝酸,烧碱,氯化铵 |
| C、冰醋酸,乙醇,醋酸钠 |
| D、盐酸,熟石灰,苛性钠 |


科目:高中化学 来源: 题型:
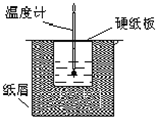 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
| 药品 | 盐酸,硫酸 | 氢氧化钠,氢氧化钙 | 红磷,硫 | 铜,锌 |
| A、甲橱 | B、乙橱 | C、丙橱 | D、丁橱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱 |
| B、电影放映时的丁达尔效应 |
| C、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
| D、在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃,1.01×105 Pa,64g SO2中含有的原子数为3NA |
| B、在常温常压下,11.2L Cl2含有的分子数为0.5NA |
| C、含有NA个氩原子的氩气在标准状况下的体积约为11.2L |
| D、标准状况下,11.2L H2O2含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有1mol HCl 生成一定有标准状况下11.2L的H2O2参加反应 |
| B、H2O2分子中既有极性共价键,又有非极性共价键,分子间又有氢键 |
| C、反应中所有的反应物、生成物都是通过共价键形成的共价化合物 |
| D、O2、O3互为同素异形体,二种晶体中微粒间的作用各不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族元素间不可能形成离子化合物 |
| B、两种简单离子不可能相差3个电子层 |
| C、同周期主族元素离子半径从左到右依次减小 |
| D、若两元素原子序数相差8,则周期数一定相差1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0L 1.0mol?L-1的NaClO水溶液中含有的氧原子数为NA |
| B、25℃时1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
| C、2.24L的2H35Cl分子中的中子数是1.9NA |
| D、某密闭容器中盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,形成N-H键的数目为0.6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com