
��������3���Ȼ�ѧ����ʽ��
2H2S(g)+3O2(g)��2SO2(g)+2H2O(l) ��H���DQ1 kJ/mol
2H2S(g)+O2(g)��2S (s)+2H2O(l) ��H���DQ2 kJ/mol
2H2S(g)+O2(g)��2S (s)+2H2O(g) ��H���DQ3 kJ/mol
�ж�Q1��Q2��Q3���߹�ϵ��ȷ����
A�� Q1>Q2>Q3 B�� Q1>Q3>Q2 C�� Q3>Q2>Q1 D�� Q2>Q1>Q

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
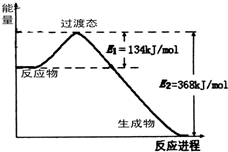 ��Դ�ǹ��÷�չ����Ҫ�������ҹ�Ŀǰʹ�õ���Դ��Ҫ�ǻ�ʯȼ�ϣ�
��Դ�ǹ��÷�չ����Ҫ�������ҹ�Ŀǰʹ�õ���Դ��Ҫ�ǻ�ʯȼ�ϣ� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�긣��ʡ������һѧ���������⿼�Ի�ѧ�Ծ� ���ͣ�ѡ����
��������3���Ȼ�ѧ����ʽ��
2H2S(g)+3O2(g)=2SO2(g)+2H2O(1) ��H=��akJ��mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(1) ��H=��bkJ��mol-1
2H2S(g)+O2(g)=2S(s)+2H2O(g) ��H=��ckJ��mol-1 ��a��b��c��������
��a��b��c���ߴ�С��ϵ���ж���ȷ����
A��a>b>c B��a>c>b C��c>b>a D��b>a>c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��㶫ʡ÷���и߶�10�¿���ѧ ���ͣ�ѡ����
��������3���Ȼ�ѧ����ʽ��
2H2S(g)+3O2(g)��2SO2(g)+2H2O(l) ��H��Q1 kJ��mol-1
2H2S(g)+O2(g)��2S (s)+2H2O(l) ��H��Q2 kJ��mol-1
2H2S(g)+O2(g)��2S (s)+2H2O(g) ��H��Q3 kJ��mol-1
�ж�Q1��Q2��Q3���߹�ϵ��ȷ���ǣ� ��
A�� Q1>Q2>Q3 B��Q1>Q3>Q2
C�� Q3>Q2>Q1 D�� Q2>Q1>Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�����������ʮ���и߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
��������3���Ȼ�ѧ����ʽ��

�ж�Q1��Q2��Q3���߹�ϵ��ȷ����
A��Q1 Q2
Q2 Q3
B��Q1
Q3
B��Q1 Q3
Q3 Q2
Q2
C��Q3 Q2
Q2 Q1
D��Q2
Q1
D��Q2 Q1
Q1 Q3
Q3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com