
分析 求出氢气的物质的量,然后根据1mol锌~2mol电子~1mol氢气,设消耗锌的物质的量为xmol,根据方程式来计算.
解答 解:生成的4.48L氢气的物质的量n=$\frac{4.48L}{22.4L/mol}$=0.2mol,设消耗锌的物质的量为xmol,可知:
1mol锌~2mol电子~1mol氢气
1 1
xmol 0.2mol
故有:$\frac{1}{xmol}=\frac{1}{0.2mol}$
解得x=0.2mol
故质量m=0.2mol×65g/mol=13g.
答:消耗锌的质量是13g.
点评 本题考查化学方程式的有关计算,为高频考点,明确各个物理量之间的关系式是解本题关键,为易错点.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:解答题
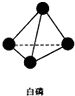 ,并指出1mol白磷(P4)含有P-P键的数目6NA
,并指出1mol白磷(P4)含有P-P键的数目6NA查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 蒸发 | B. | 蒸馏 | C. | 过滤 | D. | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
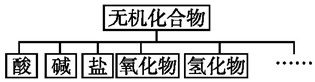
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
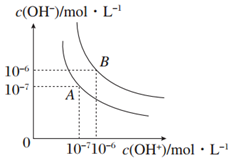 回答下列问题
回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的NaCl溶液是指由1mol NaCl和1000mL水配制成的溶液 | |
| B. | 从1L 0.5mol•L-1的NaCl溶液中取出100mL,剩余溶液物质的量浓度为0.45mol•L-1 | |
| C. | 标准状况下,18克H2O所含的氧原子数目为NA | |
| D. | 0℃时,2mol Cl2的体积不可能为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
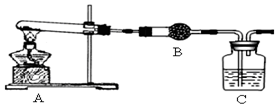
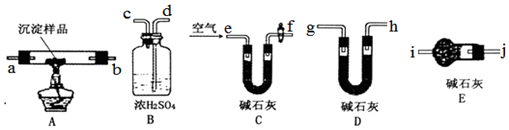
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+ NO3- I-SO42- | B. | MnO4- K+NO3-Na+ | ||
| C. | K+Al3+Cl-SO42- | D. | Mg2+SO32-Br-Ba2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com