
【题目】(1)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,写出298K时由石墨和H2(g)生成乙炔的反应的热化学方程式__________________。
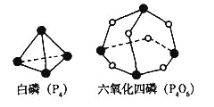
(2)化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198kJ·mol-1、P-O 360kJ·mol-1、氧气分子内氧原子间的键能为498kJ·mol-1。则P4(s)+ 3O2(g) ==P4O6(s)的反应热H为______。
(3)下图是一个电化学过程的示意图。
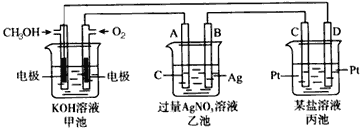
请回答下列问题:
①图中甲池是_______(填“原电池”或“电解池”)。
②A(石墨)电极的名称是_______(填“正极”“负极”“阴极”或“阳极”)。
③写出通入CH3OH的电极的电极反应式:__________________。
④乙池中反应的化学方程式为______________________,当乙池中B(Ag)极质量增加5.4 g,甲池中理论上消耗O2的体积为_________L(标准状况)。
【答案】2C(s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ/mol-1638 kJ/mol原电池阳极CH3OH+8OH--6e-=CO32-+6H2O4AgNO3+2H2O![]() 4Ag+O2↑+4HNO30.28
4Ag+O2↑+4HNO30.28
【解析】
(1)已知:①C (s,石墨)+O2(g)=CO2(g)△H1=-393.5kJmol-1;②2H2(g)+O2(g)=2H2O (l)△H2=-571.6kJmol-1;③2C2H2(g)+5O2(g)═4CO2(g)+2H2O (l)△H2=-2599kJmol-1;2C (s,石墨)+H2(g)=C2H2(g)的反应可以根据①×2+②×![]() -③×
-③×![]() 得到,所以反应焓变△H=2×(-393.5kJmol-1)+(-571.6kJmol-1)×
得到,所以反应焓变△H=2×(-393.5kJmol-1)+(-571.6kJmol-1)×![]() -(-2599kJmol-1)×
-(-2599kJmol-1)×![]() =+226.7kJmol-1,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g) △H=+226.7kJmol-1,故答案为:2C (s,石墨)+H2(g)=C2H2(g) △H=+226.7kJmol-1;
=+226.7kJmol-1,298K时由C(石墨,s)和H2(g)生成C2H2(g)反应的热化学方程式:2C (s,石墨)+H2(g)=C2H2(g) △H=+226.7kJmol-1,故答案为:2C (s,石墨)+H2(g)=C2H2(g) △H=+226.7kJmol-1;
(2)各化学键键能为P-P198kJmol-1、P-O360kJmol-1、O=O498kJmol-1,反应热△H=反应物总键能-生成物总键能,所以反应P4+3O2=P4O6的反应热△H=6×198kJmol-1+ 3×498kJmol-1- 12×360kJmol-1 =-1638kJmol-1,故答案为:-1638kJmol-1;
(3)①甲池中甲醇和氧气能自发的进行氧化还原反应,所以属于原电池,故答案为:原电池;
②乙是电解池,甲为原电池,通氧气的是正极,A和正极相连,为电解池中的阳极,故答案为:阳极;
③燃料电池中,负极上通入燃料,碱性条件下,甲醇水中和氢氧根离子反应生成碳酸根离子和水,所以电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O,故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
④乙池是电解池,碳作阳极,银作阴极,所以反应是电解硝酸银溶液,电池反应式为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3,乙池是电解池,B极上银离子得电子发生还原反应而析出银,根据转移电子相等,当乙池中B极的质量增加5.4g时,甲池中理论上消耗O2的体积=
4Ag+O2↑+4HNO3,乙池是电解池,B极上银离子得电子发生还原反应而析出银,根据转移电子相等,当乙池中B极的质量增加5.4g时,甲池中理论上消耗O2的体积=![]() ×22.4L/mol=0.28L,故答案为:4AgNO3+2H2O
×22.4L/mol=0.28L,故答案为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3;0.28。
4Ag+O2↑+4HNO3;0.28。


科目:高中化学 来源: 题型:
【题目】在120℃,101kPa条件下,由H2、CH4、CO组成的混合气体a mL,通入一定量(设为x mL)氧气使其完全燃烧。
(1)若a mL混合气体完全燃烧消耗相同条件下氧气的体积也为a mL(即x=a),则原混合气体中CH4的体积分数是____________。
(2)若完全燃烧后生成CO2和H2O(g)的总体积在相同条件下为2a mL,则原混合气体中CH4的体积分数是__________,现要测定原混合气体中H2的体积分数,还必须知道相同条件下其它数据可以是__________(填选项字母)。
A.前面提供的数据已经足够 B.生成CO2气体的总体积
C.生成H2O(g)的总质量 D.2a mL混合气体的密度
(3)若原混合气体完全燃烧时,生成的气体中只有CO2和H2O(g),求x的取值范围_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知CH3COONH4溶液呈中性,又知CH3COOH溶液加到NaHCO3溶液中有气体放出,试推断常温下NH4HCO3溶液的pH______7(填“>”、“<”或“=”)。
(2)常温下,在200 mL氢氧化钡溶液中含有1×10-3mol的钡离子,将此溶液与pH=3的盐酸混合,使其混合溶液的pH=7,应取氢氧化钡溶液和盐酸的体积之比是_________。
(3)25℃时,利用pH试纸测得0.1molL-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为_______;向10mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,溶液中c(H+)/c(CH3COOH)的值将_____(填“增大”、“减小”或“无法确定”)。
(4)电化学法是合成氨的一种新方法,其原理如图所示,阴极的电极反应式是_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是国民经济发展的重要材料,铝在地壳中的含量约占8%,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(Ⅰ)实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:Al![]() Al3+
Al3+![]() Al(OH)3↓
Al(OH)3↓
方案2:Al![]() AlO
AlO![]()
![]() Al(OH)3↓
Al(OH)3↓
方案3: ―→Al(OH)3
―→Al(OH)3
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案________。
(Ⅱ)工业上冶炼铝的流程图如图所示:

在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe2O3质量分数的数据如下:

(1)书写化学方程式,反应①________,反应②________。
(2)电解氧化铝生产铝时,阳极的电极反应式为_______________________________________。
(3)假设其他杂质不参加反应,则每生产3.4 t纯净的氧化铝,需铝土矿________t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在恒容密闭容器中,能表示反应X+2Y![]() 2Z一定达到化学平衡状态的是
2Z一定达到化学平衡状态的是
A. Z(气体)的浓度不再发生变化 B. X、Y、Z的物质的量之比是1∶2∶2
C. 容器气体的总压强不再发生变化 D. 单位时间内生成n mol Z,同时消耗2n mol Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】15g某饱和一元醇和足量金属钠反应,生成0.25 g氢气,此醇的结构简式可能是_______________和_______________。用含同位素18O的甲醇与浓硫酸和冰醋酸混合加热,其化学方程式为__________________________________________________。生成有机物的名称为_________,在反应中甲醇提供羟基上的氢原子,醋酸提供__________,从而结合生成水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Na2O与Na2O2均可与盐酸反应,故都是碱性氧化物
B.Na2O2在和CO2的反应中既作氧化剂又作还原剂
C.Na2O与H2O反应为化合反应,而Na2O2与H2O反应属于复分解反应
D.在呼吸面具中,Na2O常作供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组进行如下实验:
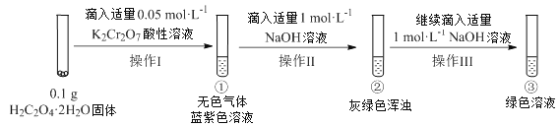
已知:Cr2(SO4)3稀溶液为蓝紫色;Cr(OH)3为灰绿色固体,难溶于水。
下列关于该实验的结论或叙述不正确的是
A. ①中生成蓝紫色溶液说明K2Cr2O7在反应中表现了氧化性
B. 若继续向③中加入稀硫酸,溶液有可能重新变成蓝紫色
C. 将①与③溶液等体积混合会产生灰绿色浑浊,该现象与Cr3+的水解平衡移动有关
D. 操作I中产生的无色气体是CO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com