
| A、稀硫酸、氯化钡溶液 |
| B、硫酸亚铁溶液、氢氧化钠溶液 |
| C、氯化钠溶液、硝酸银溶液 |
| D、氯化铝溶液、氢氧化钠溶液 |


科目:高中化学 来源: 题型:
| A、K+、NH4+、SO42-、NO3- |
| B、K+、Na+、Cl-、AlO2- |
| C、K+、Na+、Cl-、NO3- |
| D、Al3+、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④ | B、②④ | C、①④ | D、①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
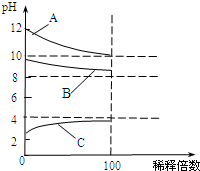 现有常温时浓度相同的五种电解质溶液:
现有常温时浓度相同的五种电解质溶液:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.9~7.1 |
| B、3.3~10.7 |
| C、4.3~9.7 |
| D、6~8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量①与②分别与少量的锌(大小相同)反应时,开始时刻速率相同,反应中速率:①<② |
| B、将②、③两种溶液混合后,若呈中性,则消耗溶液的体积:②>③ |
| C、等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D、将③稀释a倍,将④稀释b倍,两溶液pH相等,则a<b倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 提示:由8molS形成8mol S-S可推知平均1molS含有的S-S,然后计算),则Q=
提示:由8molS形成8mol S-S可推知平均1molS含有的S-S,然后计算),则Q=查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com