
【题目】![]() 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中![]() 的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
的含量变化来检测核电站是否发生放射性物质泄漏。下列有关![]() 的叙述中错误的是
的叙述中错误的是
A.![]() 的化学性质与
的化学性质与![]() 相同B.
相同B.![]() 与
与![]() 是同一种核素
是同一种核素
C.![]() 的中子数为78D.
的中子数为78D.![]() 与
与![]() 互为同位素
互为同位素
科目:高中化学 来源: 题型:
【题目】某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置如图所示(已知NO、NO2能与NaOH溶液反应):
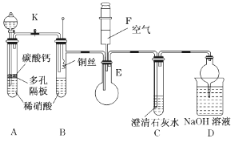
(1)设计装置A的目的是_____________________________________,为达此目的应进行的操作______________________________________________________。
(2)在(1)中的操作后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是____________________________________________________________;B中反应的离子方程式是_____________________________________________________。
(3)将注射器F中的空气推入E中,E中的气体变为红棕色,该实验的目的是____________。
(4)D装置的作用是_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(密度为1.84g·cm-3)配制成浓度为0.5mol·L-1的稀硫酸500毫升.
(1)选用的主要仪器除了烧杯、玻璃棒、胶头滴管外还有:_______________(写两个)
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.稀释浓H2SO4
E.将溶液转入容量瓶
其操作正确的顺序依次为____________________________。
(3)简要回答下列问题:
①98%的浓硫酸的物质的量浓度为_____________mol·L-1
②配制成浓度为0.5mol·L-1的稀硫酸500毫升.所需98%的浓硫酸的体积为____________mL;(保留小数点后一位)
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是_____;
④定容时必须使溶液凹液面与刻度线相切,若仰视刻度则使浓度___________。(“偏高”、“偏低”、“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

(1)装置B中盛放饱和NaCl溶液,该装置的主要作用是_________;F中的试剂是__________。
(2)实验步骤:如图连接装置后,先___________(填实验操作),再装药品,然后点燃________(填“ A” 或“C” )处酒精灯,当_________(填实验现象)时,再点燃另一处酒精灯。
(3)写出装置G 中发生反应的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________;Z的核外电子排布式是________;
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式________;
(3)D和Y形成的化合物,其分子的空间构型为________;D原子的轨道杂化方式是________;
(4)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在室温下进行下图所示实验。(已知:H2C2O4为二元弱酸)
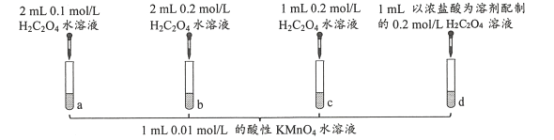
试管a、b、c中溶液褪色分别耗时690s、677s、600s。下列说法正确的是
A.反应的离子方程式为2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
B.试管c反应至300 s时,溶液中剩余的c(KMnO4)=0.0025 mol/L
C.对比试管a、b,得到的结论是H2C2O4水溶液浓度增大,反应速率加快
D.对比试管c、d,可验证H+浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯氏制碱原理:NH3+CO2+H2O+NaCl===NaHCO3↓+NH4Cl,需经过制取氨气、制取NaHCO3、分离及干燥NaHCO3四个步骤,下列图示装置能达到实验目的的是
A. 制取氨气 B. 制取NaHCO3
B. 制取NaHCO3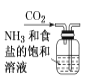
C. 分离NaHCO3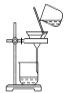 D. 干燥NaHCO3
D. 干燥NaHCO3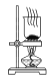
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TPE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TPE的两条合成路线(部分试剂及反应条件省略):
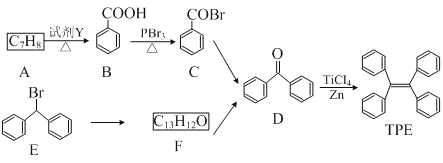
(1)A的名称是__________________;试剂Y为____________________。
(2)B→C的反应类型为_______________;B中官能团的名称是_________________,D中官能团的名称是_______________。
(3)E→F的化学方程式是______________________________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:______________________。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:______________________。
(5)下列叙述正确的是______。
a. B的酸性比苯酚强
b. D不能发生还原反应
c. E含有3种不同化学环境的氢
d. TPE既属于芳香烃也属于烯烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com