
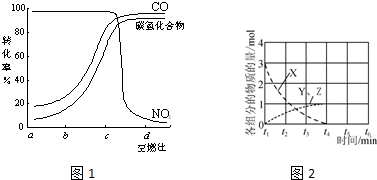
·ÖĪö £Ø1£©NOŗĶCOµÄ×Ŗ»ÆĀŹŌ½øߣ¬“߻Ɗ§¹ūŌ½ŗĆ£»
£Ø2£©·“Ó¦²śĪļNaNO2”¢NaNO3£¬øł¾ŻNaŗĶNŌ×ÓŹŲŗć£¬n£ØNaOH£©=$\frac{2.24L}{22.4L/mol}$=0.1mol£¬“ųČėc=$\frac{n}{V}$¼ĘĖćÅØ¶Č£»
£Ø3£©NOŌŚ40”ęĻĀ·Ö½āÉś³ÉĮ½ÖÖ»ÆŗĻĪļ£¬øł¾ŻŌŖĖŲŹŲŗćæÉÖŖÉś³ÉµÄĪŖNµÄŃõ»ÆĪļ£¬ÓÉĶ¼ĻóæÉÖŖ3molNOÉś³ÉĮ½ÖÖµŖµÄŃõ»ÆĪļø÷ĪŖ1mol£¬øł¾ŻŌ×ÓŹŲŗćÅŠ¶Ļ²śĪļ£®
½ā“š ½ā£ŗ£Ø1£©ŌŚcµćŹ±NOŗĶCOµÄ×Ŗ»ÆĀŹ×īøߣ¬“߻Ɗ§¹ū×īŗĆ£¬
¹Ź“š°øĪŖ£ŗc£»
£Ø2£©·“Ó¦²śĪļNaNO2”¢NaNO3£¬øł¾ŻNaŗĶNŌ×ÓŹŲŗć£¬n£ØNaOH£©=$\frac{2.24L}{22.4L/mol}$=0.1mol£¬NaOHČÜŅŗĪļÖŹµÄĮæÅضČc=$\frac{0.1mol}{0.2L}$=0.5mol/L£¬
¹Ź“š°øĪŖ£ŗ0.5mol/L£»
£Ø3£©NOŌŚ40”ęĻĀ·Ö½āÉś³ÉĮ½ÖÖ»ÆŗĻĪļ£¬øł¾ŻŌŖĖŲŹŲŗćæÉÖŖÉś³ÉµÄĪŖNµÄŃõ»ÆĪļ£¬µŖŌŖĖŲµÄŃõ»ÆĪļÓŠNO”¢N2O”¢NO2”¢N2O3”¢N2O4”¢N2O5£¬ÓÉĶ¼ĻóæÉÖŖ3molNOÉś³ÉĮ½ÖÖµŖµÄŃõ»ÆĪļø÷ĪŖ1mol£¬Ęä·“Ó¦·½³ĢŹ½ĪŖ£ŗ3NO=Y+Z£¬øł¾ŻŌ×ÓŹŲŗćæÉÖŖĪŖN2O”¢NO2£¬
¹Ź“š°øĪŖ£ŗN2O”¢NO2£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ÓėĶ¼Ļó”¢Ō×ÓŹŲŗćĖ¼Ļė”¢Ķ¼ĻóµÄ·ÖĪöÓėÓ¦ÓĆµČ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŅŌ¼°¶Ō»ł“”ÖŖŹ¶µÄ×ŪŗĻÓ¦ÓĆÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
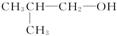
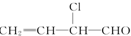
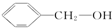
| A£® | ¢Ś¢Ū¢Ż | B£® | ¢Ś¢Ü¢Ž | C£® | ¢Ū¢Ü¢Ž | D£® | ¢Ł¢Ś¢Ū¢Ü¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | ŹŅĪĀĻĀ£¬ŹŌ¹ÜÖŠĖł¼ÓŹŌ¼Į¼°ĘäÓĆĮæ/mL | ŹŅĪĀĻĀČÜŅŗŃÕÉ«ĶŹÖĮĪŽÉ«ĖłŠčŹ±¼ä/min | |||
| 0.6 mol/L H2C2O4ČÜŅŗ | H2O | 0.2 mol/L KMnO4ČÜŅŗ | 3 mol/L Ļ”ĮņĖį | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
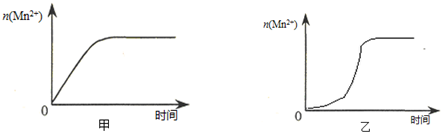
| ŹµŃ鱹ŗÅ | ŹŅĪĀĻĀ£¬ŹŌ¹ÜÖŠĖł¼ÓŹŌ¼Į¼°ĘäÓĆĮæ/mL | ŌŁĻņŹŌ¹ÜÖŠ¼ÓČėÉŁĮæ¹ĢĢå | ŹŅĪĀĻĀČÜŅŗŃÕÉ«ĶŹÖĮĪŽÉ«ĖłŠčŹ±¼ä/min | |||
| 0.6 mol/L H2C2O4ČÜŅŗ | H2O | 0.2 mol/L KMnO4ČÜŅŗ | 3 mol/L Ļ”ĮņĖį | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
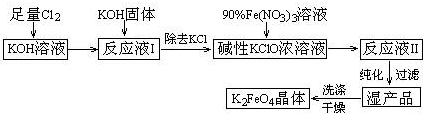
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
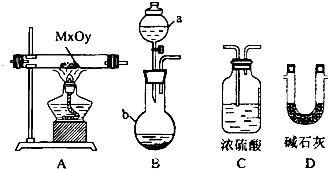
| ŠņŗÅ | ¹ĢĢå³É·Ö£ØĢī»ÆѧŹ½£© |
| 1 | |
| 2 | |
| 3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
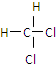 ŗĶ
ŗĶ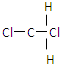
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
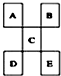
| A£® | DŅ»¶ØŹĒ½šŹōŌŖĖŲ£¬Ę佚ŹōŠŌ±ČCĒæ | |
| B£® | CµÄ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļĻŌĒæĖįŠŌ | |
| C£® | BµÄĒā»ÆĪļŹĒŅŌ·Ö×ÓŠĪŹ½“ęŌŚ£¬ĒŅijŠ©·Ö×Ó¼ä“ęŌŚĒā¼ü | |
| D£® | EµÄŌ×ÓŠņŹżŅ»¶ØŹĒAµÄ5±¶£¬ĒŅŌ×Ó°ė¾¶±ČA“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com