
分析 (1)根据n=cV分别计算出氯化钡、硝酸银的物质的量,然后结合反应方程式判断过量情况,根据不足量计算出生成氯化银的物质的量;
(2)根据过量情况计算出反应后溶液中氯离子的物质的量,再根据c=$\frac{n}{V}$计算出氯离子浓度.
解答 解:(1)n(AgNO3)=0.5mol/L×0.5L=0.25mol,n(BaCl2)=0.5mol/L×0.5L=0.25mol,
二者反应方程式为:2AgNO3 +BaCl2═Ba(NO3)2+2AgCl↓,
则氯化钡不足,反应生成氯化银的物质的量为:n(AgCl)=n(AgNO3)=0.25mol,
答:生成氯化银沉淀的物质的量为0.25mol;
(2)反应剩余的氯离子的物质的量为:0.25mol×2-0.25mol=0.25mol,
则反应后溶液中Cl-的物质的量浓度为:c(Cl-)=$\frac{0.25mol}{0.5L+0.5L}$=0.25mol/L,
答:反应后Cl-的物质的量浓度为0.25mol/L.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确发生反应的实质为解答关键,注意熟练掌握物质的量与物质的量浓度之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
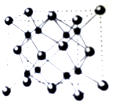 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
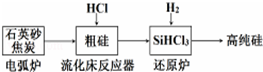
| 发生的主要反应 | |
| 电弧炉 | SiO2+2C$\frac{\underline{\;1600-1800℃\;}}{\;}$si+2CO |
| 流化床反应器 | Si+3HCl$\frac{\underline{\;250-300\;}}{\;}$SiHCl3+H2 |
| 还原炉 |
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/°C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 温度/K | 锌 | c(Zn2+)/mol/L | c(H+)/mol/L | 另加溶液 |
| A | 281 | 锌块 | 0.1 | 3 | |
| B | 308 | 锌粉 | 0.2 | 3 | 少量氯化铜 |
| C | 281 | 锌块 | 0.1 | 2 | |
| D | 308 | 锌粉 | 0.1 | 3 | 少量氯化钡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、CO32-、NO3- | B. | Cu2+、Cl-、OH- | C. | Na+、Cl-、HCO3- | D. | Ag+、K+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com