
| A. | 改用锌粉 | B. | 滴入几滴硫酸铜溶液 | ||
| C. | 加入少量1mol•L-1稀硫酸 | D. | 加入少量NaCl溶液 |
分析 根据影响化学反应速率的因素分析,若增大反应速率,可以升高温度、增大锌的表面积、增大氢离子浓度等,而加入少量氯化钠溶液,导致原溶液中氢离子浓度减小,反应速率减小,据此进行解答.
解答 解:A.锌片改为锌粉,增大了锌的接触面积,可以加快反应速率,故A不选;
B.锌与滴入几滴硫酸铜溶液反应生成少量的铜,构成锌铜原电池加快化学反应速率,故B不选;
C.加入1mol/L的稀硫酸,增大了溶液中氢离子浓度,从而加快了反应速率,故C不选;
D.加入少量氯化钠溶液,钠离子和氯离子不需要锌与氢离子的反应,而原溶液中氢离子浓度减小,导致反应速率减小,故D选;
故选D.
点评 本题考查了化学反应速率及其影响因素,题目难度不大,明确影响化学反应速率的因素为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | Cu与Cl2直接化合生成CuCl2;Cu与S直接化合也能得到CuS | |
| B. | Fe3O4可写成FeO•Fe2O3;Pb3O4也可写成PbO•Pb2O3 | |
| C. | Mg失火不能用CO2灭火;Na失火也不能用CO2灭火 | |
| D. | 工业上电解熔融MgCl2制取金属镁;也用电解熔融AlCl3的方法制取金属铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
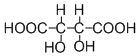
| A. | 酒精可以和水以任意比例互溶,与氢键有关 | |
| B. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,与氢键有关 | |
| C. | 无机含氧酸的化学式可以用XOn(OH)m表示,n值越大,则该酸的酸性就越强.则可推知,硫酸酸性强于磷酸 | |
| D. | 如图该分子中没有手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .如果要合成
.如果要合成 ,所用的原始原料可以是( )
,所用的原始原料可以是( )| A. | 2,3-二甲基-1,3-丁二烯和乙烯 | B. | 2,3-二甲基-1,3-丁二烯和乙炔 | ||
| C. | 1,3-丁二烯和2-丁炔 | D. | 1,3-丁二烯和2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
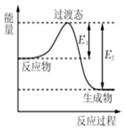 如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )
如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )| A. | 若在反应体系中加入催化剂,E1不变 | |
| B. | 活化能的大小决定了反应热的大小 | |
| C. | 该反应的活化能等于ykJ/mol | |
| D. | 1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)的△H=(x-y)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲是苯的同系物,乙不是苯的同系物,甲乙瓦为同分异构体 | |
| B. | 甲、乙均能发生取代反应和加成反应 | |
| C. | 甲的一氯代物有2种,乙的一氯代物有7种(不考虑顺反异构) | |
| D. | 甲分子中所有原了可能在同一平面上,乙分子中所有原了一定在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
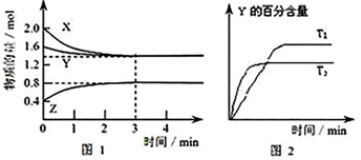
| A. | 容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | |
| B. | 反应进行的前3 min内,用X表示的反应速率 v(X)=0.3mol/(L•min) | |
| C. | 据图2可知,相对于T1,温度为T2时更快达到“拐点”,说明T2时化学反应速率更快,可确定温度T2高于T1 | |
| D. | 若改变反应条件,使反应进程如图3所示,则改变的条件可能是使用了催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com