
����Ŀ����Ԫ�غ�±��Ԫ�ض����γɶ������ʣ����ǿ���������ѧ���ʽṹ�����ʵ����֪ʶȥ��ʶ�����⣮
��1����ļ۵����Ų�ʽΪ��PCl3�Ŀռ乹��Ϊ ��
��2����֪CsICl2���ȶ��������ֽ⣬���������ɾ����ܸ�������ʣ����������� ʽ������
A.CsICl2=CsCl+ICl
B.CsICl2=CsI+Cl2
��3�������±��ṩ�ĵ�һ�����������жϣ����п������ɽ��ȶ��ĵ��������ӵ�±��ԭ���� ��
�� | �� | �� | �� | |
��һ�����ܣ�kJmol��1�� | 1681 | 1251 | 1140 | 1008 |
��4�����з��ӼȲ�����s��p�Ҽ���Ҳ������p��p�м����� ��
A.HCl
B.HF
C.SO2
D.SCl2
��5����֪COCl2Ϊƽ���Σ���COCl2����̼ԭ�ӵ��ӻ��������Ϊ �� д��CO�ĵȵ����������д��1������
��6������������ȼ��ʱ�õ�һ�ָƵ������ᄃ�壬��ṹ��ͼ��ʾ���ɴ˿��жϸøƵ�������Ļ�ѧʽΪ ����֪����������ܶ��Ǧ�gcm��3 �� �������������������Ӽ�ľ���Ϊ cm��ֻҪ������ʽ�����ؼ������ֵ�������ӵ�����ΪNA����
���𰸡�
��1��4s24p5��������
��2��A
��3����
��4��D
��5��sp2�ӻ���N2
��6�� CaO2��![]()
����������1���崦�ڵ������ڢ�A�壬�۵����Ų�ʽΪ4s24p5��PCl3��Pԭ�ӹµ��Ӷ���= ![]() =1���۲���Ӷ���=3+1=4�����ӿռ乹��Ϊ�����Σ� �ʴ�Ϊ��4s24p5�������Σ���2��CsICl2���ȶ��������ֽ⣬���������ɾ����ܸ�������ʣ����������ӵİ뾶С�ڵ����ӣ�����CsCl�ľ����ܴ���CsI�ľ����ܣ�����ӦCsICl2=CsCl+ICl���У���ѡ��A����3��I�ĵ�һ������ԽС����������γɽ��ȶ��ĵ��������ӣ��ʴ�Ϊ���⣻��4��A�� HCl��Ϊ����������s��p�Ҽ���B��HF��Ϊ����������s��p�Ҽ���C�� SO2�к���˫��������p��p�м���D�� SCl2��Ϊ����������p��p�Ҽ����ʴ�Ϊ��D����5��COCl2Ϊƽ���Σ���ṹʽ��
=1���۲���Ӷ���=3+1=4�����ӿռ乹��Ϊ�����Σ� �ʴ�Ϊ��4s24p5�������Σ���2��CsICl2���ȶ��������ֽ⣬���������ɾ����ܸ�������ʣ����������ӵİ뾶С�ڵ����ӣ�����CsCl�ľ����ܴ���CsI�ľ����ܣ�����ӦCsICl2=CsCl+ICl���У���ѡ��A����3��I�ĵ�һ������ԽС����������γɽ��ȶ��ĵ��������ӣ��ʴ�Ϊ���⣻��4��A�� HCl��Ϊ����������s��p�Ҽ���B��HF��Ϊ����������s��p�Ҽ���C�� SO2�к���˫��������p��p�м���D�� SCl2��Ϊ����������p��p�Ҽ����ʴ�Ϊ��D����5��COCl2Ϊƽ���Σ���ṹʽ�� ![]() ��Cԭ�ӵ��ӻ������ĿΪ3���ӻ�����Ϊsp2�ӻ���CO�ĵȵ��������Ϊ��N2�ȣ��ʴ�Ϊ��sp2�ӻ���N2����6�������и����ӵĸ���Ϊ8��
��Cԭ�ӵ��ӻ������ĿΪ3���ӻ�����Ϊsp2�ӻ���CO�ĵȵ��������Ϊ��N2�ȣ��ʴ�Ϊ��sp2�ӻ���N2����6�������и����ӵĸ���Ϊ8�� ![]() +6��
+6�� ![]() =4���������ӵĸ���Ϊ12��
=4���������ӵĸ���Ϊ12�� ![]() +1=4�����仯ѧʽΪCaO2 �� ��������Ϊ4��
+1=4�����仯ѧʽΪCaO2 �� ��������Ϊ4�� ![]() g���辧���ı߳�Ϊacm����a cm��3����gcm��3=4��
g���辧���ı߳�Ϊacm����a cm��3����gcm��3=4�� ![]() g����a=
g����a= ![]() �������������ĸ���λ�ڶ���������ϵģ����ǵľ���Ϊ�����߳���
�������������ĸ���λ�ڶ���������ϵģ����ǵľ���Ϊ�����߳��� ![]() ����Ϊ
����Ϊ ![]() ��
�� ![]() cm���ʴ�Ϊ��CaO2��
cm���ʴ�Ϊ��CaO2�� ![]() ��
�� ![]() cm����1���崦�ڵ������ڢ�A�壻PCl3��Pԭ�ӹµ��Ӷ���=
cm����1���崦�ڵ������ڢ�A�壻PCl3��Pԭ�ӹµ��Ӷ���= ![]() =1���۲���Ӷ���=3+1=4����2�������Ӿ��������Ӱ뾶ԽС�������������Խ�ߣ�������Խ��3����һ��������ָԭ��ʧȥһ�������������������һ������ԽС����Խ����ʧȥһ�����ӣ���4��s�ܼ���p�ܼ������γɵĹ��ۼ�Ϊs��p�Ҽ���p�ܼ�����֮���γ�˫���������к���p��p�м�����5��COCl2Ϊƽ���Σ���ṹʽ��
=1���۲���Ӷ���=3+1=4����2�������Ӿ��������Ӱ뾶ԽС�������������Խ�ߣ�������Խ��3����һ��������ָԭ��ʧȥһ�������������������һ������ԽС����Խ����ʧȥһ�����ӣ���4��s�ܼ���p�ܼ������γɵĹ��ۼ�Ϊs��p�Ҽ���p�ܼ�����֮���γ�˫���������к���p��p�м�����5��COCl2Ϊƽ���Σ���ṹʽ�� ![]() ��Cԭ�ӵ��ӻ������ĿΪ3���ȵ������Ǿ�����ͬ�ļ۵���������ͬԭ������������6�����ݾ�̯��ȷ�������и���ԭ�ӵĸ�������ȷ���仯ѧʽ�����㾧������������ܶ�ȷ�������������������þ����ı߳��������������ĸ���λ�ڶ���������ϵģ����ǵľ���Ϊ�����߳���
��Cԭ�ӵ��ӻ������ĿΪ3���ȵ������Ǿ�����ͬ�ļ۵���������ͬԭ������������6�����ݾ�̯��ȷ�������и���ԭ�ӵĸ�������ȷ���仯ѧʽ�����㾧������������ܶ�ȷ�������������������þ����ı߳��������������ĸ���λ�ڶ���������ϵģ����ǵľ���Ϊ�����߳��� ![]() ��
��


 ����С����ͬ������ϵ�д�
����С����ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����15�֣��غ͵����ػ������ڻ�����ҽҩ�����ϵ��������Ź㷺��Ӧ�ã��ش��������⣺
��1��Ԫ��K����ɫ��Ӧ���Ϻ�ɫ��������ɫ��Ӧ�ķ��䲨��Ϊnm�����ţ���
A.404.4
B.553.5
C.589.2
D.670.8
E.766.5
��2����̬Kԭ���У��������ռ�ݵ�����ܲ�ķ����� �� ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ �� K��Cr����ͬһ���ڣ��Һ����������ӹ�����ͬ��������K���۵㡢�е�ȶ��Ƚ���Cr�ͣ�ԭ���� ��
��3��X��������ⶨ�ȷ��֣�I3AsF6�д���I3+���ӣ�I3+���ӵļ��ι���Ϊ �� ����ԭ�ӵ��ӻ�����Ϊ ��
��4��KIO3������һ���������õķ����Թ�ѧ���ϣ����и��ѿ��͵�����ṹ���߳�Ϊa=0.446nm��������K��I��O�ֱ��ڶ��ǡ����ġ�����λ�ã���ͼ��ʾ��K��O�����̾���Ϊnm����K���ڵ�O����Ϊ ��
��5����KIO3�����ṹ����һ�ֱ�ʾ�У�I���ڸ�����λ�ã���K����λ�ã�O����λ�ã�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȳ��һ����Ҫ���л�����ԭ�ϣ�����ȲΪԭ���ڲ�ͬ�ķ�Ӧ�����¿���ת�������»��������˵����ȷ���ǣ� �� 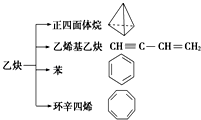
A.����������ķ���ʽΪC4H4 �� ����ȴ���������
B.����������Ȳ����ϩ����Ȳ��ȫȼ��ʱ�ĺ�������ͬ
C.��Ϊƽ�������νṹ�������д���C��C��C�TC����ʹ����KMnO4��Һ��ɫ
D.������ϩ�����Ľṹ������ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����жԻ����ķ��뷽����˵������ȷ����(����)
A. �е㲻ͬ��Һ̬����������������
B. �������ܵ�Һ̬�������÷�Һ��������
C. ���ܵ�Һ̬�������÷�Һ�ķ�������
D. ������ˮ�Ĺ�����������ˮ�Ĺ����γɵĻ��������ܽ⡢���ˡ������ķ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʳ����һ�ֳ��õ�ʳƷ���Ӽ��������㡢����ʳ�����պ�����ӳ������ڣ�����Ϊ (����)
A.NaCl�е�Cl����ɱ������
B.Ũʳ��ˮ�к�O2�٣�ϸ��������
C.����������ʹϸ��ʧˮ����
D.����������ʹ�㡢��ϸ��ʧˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������34gNH3 �� ��ͨ��������գ�
��1�����������ʵ���Ϊmol������Hԭ����ĿΪ ��
��2���������ڱ�״���µ����ΪL��
��3����������������ˮ���VL��Һ��������Һ���ʵ����ʵ���Ũ��Ϊmol/L��
��4��������������100mLˮ�У�������Һ���ʵ���������ԼΪ%��С�������һλС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƿ������ڸ��Ƶر�ˮ�ʣ��������ؽ������ӷ�ˮ�������ೱ��Ҳ������Ӧ�������ȣ���ҵ�������������Ƶ���Ҫ�������£� 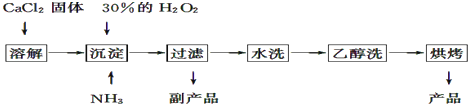
��֪CaO28H2O�ʰ�ɫ������ˮ�������ڴ�������ѵȣ�������350�����ҿ�ʼ�ֽ�ų�������
��1��������������ȡCaO28H2O�Ļ�ѧ����ʽ����
��2�����Ʒ��ĸ���ƷΪ���ѧʽ����Ϊ����߸���Ʒ�IJ��ʣ��ᾧǰҪ����Һ��pH���������ʷ�Χ���ɼ�����Լ�����
��3�����顰ˮϴ���Ƿ�ϸ�ķ�������
��4���ⶨ��Ʒ��CaO2�ĺ�����ʵ�鲽�裺
��һ����ȷ��ȡa g��Ʒ��������ƿ�У�������������ˮ������b g KI���壬�ٵ�������2molL��1��������Һ����ַ�Ӧ��
�ڶ�������������ƿ�м��뼸�ε�����Һ��
����������μ���Ũ��Ϊc molL��1��Na2S2O3��Һ����Ӧ��ȫ������Na2S2O3��ҺV mL��
��֪��I2+2S2O32���T2I��+S4O62��
�ٵ�һ����Ӧ�����ӷ���ʽΪ��
�ڵ�������ʢ��Na2S2O3��Һ������������ �� ��Ӧ��ȫʱ������Ϊ
�۲�Ʒ��CaO2����������Ϊ������ĸ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�ĵ绯ѧװ���У��缫IΪAl�������缫��ΪCu��������˵����ȷ���ǣ� ��
A.�������缫����
B.���缫I
C.�缫��ĵ缫��Ӧ��2H2O-4e-=4H++O2��
D.�缫����������٣��缫�����������
E.�����ձ��е�SO42��Ũ�ȶ�ʼ�ձ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ƭ����Ƭ�Ϸֱ����������Һ������������������Ƭʱ���а��̲�������(����)
��Ũ���ᡡ��Ũ���ᡡ��Ũ���ᡡ��Ũ����
A. �٢� B. �٢� C. �ڢۢ� D. �ۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com