
下图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊试液,下列实验现象中正确的是
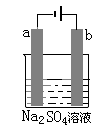
A.逸出气体的体积a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近出现蓝色
D.a电极附近呈蓝色,b电极附近出现红色
D
【解析】
试题分析:a连接电源的负极,为电解池的阴极,b连接电源的正极,为电解池的阳极,电解Na2SO4水溶液阳极发生的反应为:4OH--4e-═2H2O+O2↑或2H2O-4e-═4H++O2↑,阴极反应为:2H++2e-═H2↑,或2H2O+2e-═H2↑+2OH-。A、a极生成氢气,b极生成氧气,二者的体积比为2:1,逸出气体的体积a电极的大于b电极的,A错误; B、两极生成的气体分别为氧气和氢气,都为无色无味气体,B错误;C、电极生成OH-离子,呈碱性,滴加石蕊呈蓝色,b电极生成H+离子,呈酸性,滴加石蕊呈红色,C错误;D、a电极生成OH-离子,呈碱性,滴加石蕊呈蓝色,b电极生成H+离子,呈酸性,滴加石蕊呈红色,D正确;答案选D。
考点:考查电解原理的应用。


科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
下面关于下图所示实验装置的使用方法中叙述正确的是
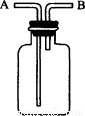
①用于排水集气:充满水,B进气,A排放水
②用于收集密度比空气大的气体:B进气,A排放空气
③用于收集密度比空气小的气体:B进气,A排放空气
④用于洗气:装入洗液,A进气,B出气
A.全正确 B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高一上学期月考化学试卷(解析版) 题型:填空题
(18分)某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题:
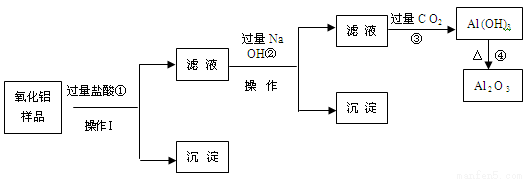
(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为:
、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高二上学期月考化学试卷(解析版) 题型:填空题
(共8分)A、B、C、D、E均为可溶于水的固体,组成他们的离子有
阳离子 | Na+ Mg2+ Al3+ Ba2+ |
阴离子 | OH- Cl- CO32- SO42- HSO4- |
分别取它们的水溶液进行实验,结果如下:①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
(1)据此推断它们是(写化学式)A ;B ;C ;D ;E 。
(2)写出④中反应的离子方程式: 。
(3)A溶液中各种离子浓度由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高二上学期月考化学试卷(解析版) 题型:选择题
下列说法正确的是
①可用Ba(OH)2溶液同时鉴别AgNO3、AlCl3、NH4Cl、NaCl、Na2SO4五种溶液
②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
③因为氧化性:HClO>H2SO4,所以非金属性:Cl>S
④胶体的本质特征是丁达尔现象
⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
A.①②⑤ B.①②④ C.②④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高二上学期月考化学试卷(解析版) 题型:选择题
反应:X(g)+3Y(g)  2Z(g) △H<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2Z(g) △H<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
A.正反应速率加大,逆反应速率变小,平衡正向移动
B.正反应速率变小,逆反应速率加大,平衡逆向移动
C.正反应速率和逆反应速率都变小,平衡正向移动
D.正反应速率和逆反应速率都变小,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省高二上学期1月质量检测化学试卷(解析版) 题型:选择题
室温时将浓度和体积分别为c1、V1的NaOH溶液和c2、V2的CH3COOH溶液相混合,下列关于该混合溶液的叙述错误的是
A.若pH>7,则一定是c1V1=c2V2
B.在任何情况下都是c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.当pH=7时,若V1=V2,则一定是c1<c2
D.若V1=V2、c1=c2,则c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高二上学期期中化学试卷(解析版) 题型:实验题
(14分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净并检查不漏水,且用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00 mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净并检查不漏水后,立即向其中注入0.1000 mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0”刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且在30 s内颜色不再变化,测得所耗盐酸的体积为V1 mL。
④重复以上过程,但在滴定过程中向锥形瓶中加入5 mL的蒸馏水,测得所耗盐酸的体积为V2 mL。
试回答下列问题:
(1)锥形瓶中的溶液从_____色变为_____色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_____。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是__________。由此造成的测定结果_____(填“偏高”、“偏低”或“无影响”)
(4)步骤②缺少的操作是__________。
(5)如图,是某次滴定时的滴定管中的液面,其读数为_____ mL。
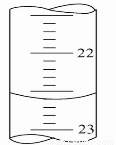
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com