
 2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����
2Z(g)�����ﵽƽ�⡣��֪����Ӧ�Ƿ��ȷ�Ӧ�����X��ת����Ϊ37. 5%��Y��ת����Ϊ25%�������й�������ȷ����| A����X�ķ�Ӧ����Ϊ0.2 mol��L��1��s��1����Z�ķ�Ӧ����Ϊ0.3 mol��L��1��s��1 |
| B�����������г��뺤����ѹǿ����Y��ת������� |
| C�������¶ȣ�����Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ� |
| D����ʼ���������е�X��Y���ʵ���֮��Ϊ2��1 |
 �żӾ���ϵ�д�
�żӾ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ˮʱ��ƽ���淴Ӧ�����ƶ� |
| B������������NaOH����,ƽ��������Ӧ�����ƶ� |
| C����������0.1 mol/L HCl��Һ,��Һ��C(H��)���� |
| D����������CH3COONa ���壬ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO��O2���˷�Ӧ�ﵽƽ��״̬ʱ�ı�־��(����)
2NO��O2���˷�Ӧ�ﵽƽ��״̬ʱ�ı�־��(����)| A������������ɫ��dz |
| B�����������ܶȲ��ٱ仯 |
| C���������NO2��NO��O2���ʵ���֮��Ϊ2��2��1 |
| D����λʱ��������2n mol NO��ͬʱ����2n mol NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 [CuCl4]2-(��)+4H2O��ʹ����ɫCuCl2��Һ����ɫת���IJ�����
[CuCl4]2-(��)+4H2O��ʹ����ɫCuCl2��Һ����ɫת���IJ�����| A������Ũ�� | B����ˮϡ�� | C������AgNO3 | D������ʳ�ξ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������8 mol | B������1.6 mol | C������0.8 mol��1.6 mol? | D������1.6 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
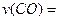 ��
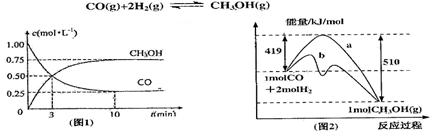
��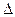 H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ�
H>0������Ӧ��д����Ӧ���Ȼ�ѧ����ʽ ��ѡ�����˵Ĵ����� ����ܡ����ܡ����ı�÷�Ӧ�ķ�Ӧ�ȣ� ��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������
��ʽΪ ���¶����ߣ�ƽ�ⳣ��K ������������䡱��С������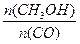 ����� ��
����� �� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
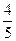 ,��N2��ת����Ϊ
,��N2��ת����Ϊ| A��50% | B��37.5% | C��25% | D��12.5% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
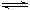 2Z(g)��X��Y��Z ����ʼŨ������Ϊ0.1 mol/L��0.3 mol/L��0.2 mol / L������Ӧ��ƽ��ʱ�������ʵ�Ũ�ȿ�����
2Z(g)��X��Y��Z ����ʼŨ������Ϊ0.1 mol/L��0.3 mol/L��0.2 mol / L������Ӧ��ƽ��ʱ�������ʵ�Ũ�ȿ�����
| A��X��0.2 mol / L | B��Y��0.5 mol  / L / L |
| C��Z��0.3 mol / L | D��Z��0.4 mol / L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2HBr(g)����֪����0.5 mol H2��1 mol Br2ʱ���ﵽƽ�������0.5a mol HBr(������֪��)����ͬ�����£��ұ���ƽ��ʱ����ֵ�����������䣬�����б��(1)��(3)��״̬����д���еĿհס�
2HBr(g)����֪����0.5 mol H2��1 mol Br2ʱ���ﵽƽ�������0.5a mol HBr(������֪��)����ͬ�����£��ұ���ƽ��ʱ����ֵ�����������䣬�����б��(1)��(3)��״̬����д���еĿհס�| ��� | ��ʼ״̬/ mol | ƽ��ʱHBr�����ʵ��� / mol | ||
| H2 | Br2 | HBr | ||
| ��֪ | 0.5 | 1 | 0 | 0.5a |
| (1) | 2 | 4 | 0 | �� |
| (2) | �� | �� | 1 | 0.5a |
| (3) | m | n(n��2m) | �� | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com