

 ��
��
���� AԪ���γ���������壬AΪHԪ�أ�B��Eͬ�壬B�ĵ����ڿ����������������B��ijЩ���������γɹ⻯ѧ��������Ҫ���ʣ�ӦΪNԪ�أ���EΪPԪ�أ�C�ǵؿ��к������ķǽ���Ԫ�أ�ӦΪOԪ�أ�D�Ƕ������е縺����С��Ԫ�أ���ΪNaԪ�أ�F������������ˮ��������ǿ���ᣬFΪClԪ�أ���϶�Ӧ���ʡ�������������Լ���ĿҪ������⣮
��� �⣺AԪ���γ���������壬AΪHԪ�أ�B��Eͬ�壬B�ĵ����ڿ����������������B��ijЩ���������γɹ⻯ѧ��������Ҫ���ʣ�ӦΪNԪ�أ���EΪPԪ�أ�C�ǵؿ��к������ķǽ���Ԫ�أ�ӦΪOԪ�أ�D�Ƕ������е縺����С��Ԫ�أ���ΪNaԪ�أ�F������������ˮ��������ǿ���ᣬFΪClԪ�أ�
��1��BΪNԪ�أ���̬ԭ�Ӽ۵����Ų�ͼΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��NO3-��N�γ�3���ļ���û�йµ��Ӷԣ�Ϊƽ�������Σ�PCl3������P�γ�3���ļ�����1���µ��Ӷԣ�Ϊ���Է��ӣ��ʴ�Ϊ��ƽ�������Σ����ԣ�
��3��N�ķǽ����Խ�ǿ����Ӧ���⻯����γ�������е�ϸߣ��ʴ�Ϊ��������֮����������
��4����H��N��O����Ԫ����ɵ����ӻ����ﻯѧʽΪNH4NO3��Ϊǿ�������Σ�ˮ������ԣ�ˮ������ӷ���ʽΪNH4++H2O?NH3��H2O+H+��
�ʴ�Ϊ��NH4NO3��NH4++H2O?NH3��H2O+H+��
��5�����ɵ�����NaCl��NH4Cl���������������Σ������ʽ�ֱ�Ϊ ��
�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
��
��6��EԪ����FԪ�����γɵ�ԭ�Ӹ�����Ϊ1��5�Ļ����ΪPCl5��������ˮ��Ӧ���������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪPCl5+4H2O=H3PO4+5HCl��
�ʴ�Ϊ��PCl5+4H2O=H3PO4+5HCl��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã�Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��Ŀ�Ѷ��еȣ��ƶ�Ԫ���ǽ���Ĺؼ���ע���Ԫ�ػ�����֪ʶ�����գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 6�� | C�� | 9 �� | D�� | 12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�Ag2SO4��AgCl��AgI��ˮ���ܽ��������μ��� | |
| B�� | ��AgCl������Һ�м���NaI���壬��AgI�������� | |
| C�� | ��AgCl������Һ�м���NaI���壬��AgI�������� | |
| D�� | ��ΪAgCl��Ag2SO4�����ܣ�����AgCl����ת��ΪAg2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 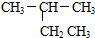 2-�һ����� | B�� | 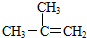 2-��-2-��ϩ | ||
| C�� | 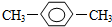 ����ױ� | D�� | CH3CH2CH2CH2OH1-���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
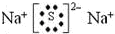
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��g��+Cl2��g���T$\frac{1}{2}$HCl��g����H=+92.4kJ/mol | B�� | H2��g��+Cl2��g���T$\frac{1}{2}$HCl��g����H=-92.4kJ/mol | ||
| C�� | H2��g��+Cl2��g���T2HCl��g����H=-184.8kJ/mol | D�� | H2��g��+Cl2��g���T2HCl��l����H=+184.8kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢܢ� | B�� | �ܢ� | C�� | �ܢݢ� | D�� | �ۢܢݢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com