
下列各组中的反应,属于同一反应类型的是
A.由乙醇与浓H2SO4制备乙烯;由乙烯与水反应制备乙醇
B.由甲苯与液溴制备邻溴甲苯;由苯制备硝基苯
C.由乙醛与O2制备乙酸;由乙醛与H2制备乙醇
D.由油酸甘油酯与H2制备硬脂酸甘油酯;由硬脂酸甘油酯制备硬脂酸
科目:高中化学 来源:2015-2016学年新疆石河子二中高二下期末化学试卷(解析版) 题型:选择题
下列与有机物结构、性质相关的叙述错误的是
A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2
B.蛋白质和油脂都属于高分子化合物,一定条件下都能水解
C.甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同
D.苯 不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高二下期末化学试卷(解析版) 题型:选择题
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )
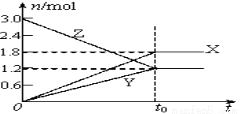
A.该反应的化学方程式为:3X+2Y 2Z
2Z
B.若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0
C.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D.若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z发生的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
已知在酸性溶液中,下列物质氧化H2S生成S是时,自身发生如下变化: IO3-→I2; Fe3+→Fe2 +; SO2→S;MnO4-→Mn2+ 。如果分别用等物质的量的这些物质氧化足量的H2S,得到S最多的是( )
A.IO3- B.Fe3+ C.SO2 D. MnO4-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
下列关于NH4+、NH3、NH2-三种微粒的说法不正确的是
A.三种微粒所含有的电子数相等
B.三种微粒中氮原子的杂化方式相同
C.三种微粒的空间构型相同
D.键角大小关系:NH4+>NH3>NH2-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一下期末化学试卷(解析版) 题型:填空题
已知N2O4和NO2可以相互转化:2NO2(g)  N2O4(g) △H<0现将一定量N2O4和NO2的混合气体通入体积为2L的恒温密闭玻璃容器中,发生反应,各物质浓度随时间变化关系如图:
N2O4(g) △H<0现将一定量N2O4和NO2的混合气体通入体积为2L的恒温密闭玻璃容器中,发生反应,各物质浓度随时间变化关系如图:
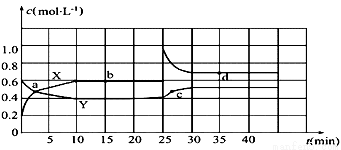
(1)图中曲线______(填“X”或“Y”)表示c(N2O4)随时间的变化。
(2)从起点开始首次达到平衡时,以NO2表示的反应速率为______。
(3)图中b点的平衡常数K的值为________。
(4)其他条件不变,若起始时向该容器中通入0.4molN2O4和0.2molNO2,则v正_____v逆(填“>”、“=”或“<”);若升温该反应的平衡常数K______(填“增大”、“减小”或“不变”) ,判断理由是_________________。
(5)25min时,改变的外界条件是______,图象中a、b、c、d四点中v正=v逆的点是____,四点中________点体系颜色最深。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一下期末化学试卷(解析版) 题型:选择题
a1、a2分别为A在甲、乙两个恒温容器中建立平衡体系A(g) 2B(g)时的转化率,已知甲容器保持压强不变,乙容器保持容器体积不变。在温度不变的情况下,均增加A的物质的量,下列判断正确的是
2B(g)时的转化率,已知甲容器保持压强不变,乙容器保持容器体积不变。在温度不变的情况下,均增加A的物质的量,下列判断正确的是
A.a1、a2均减小 B.a1减小,a2增大
C.a1不变,a2增大 D.a1不变,a2减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省等三校高一下期末化学试卷(解析版) 题型:实验题
(1)用O2将HC1转化为Cl2,可提高效益,减少污染,传统上该转化通过如下图所示的催化剂循环实现,
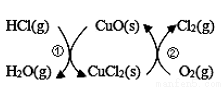
其中,反应①为:2HCl(g)+CuO(s)  H2O(g)+CuCl2(s) △H1,反应②生成1 mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为____________________________。(反应热用△H1和△H2表示)。
H2O(g)+CuCl2(s) △H1,反应②生成1 mol Cl2 (g)的反应热为△H2,则总反应的热化学方程式为____________________________。(反应热用△H1和△H2表示)。
(2)一定条件下测得上述反应过程中c(Cl2)的数据如下:
t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
c(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
计算2.0~6.0min内以HCl的物质的量浓度变化表示的反应速率 _________。
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
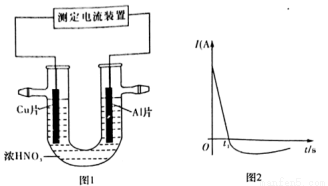
0~tl时,原电池的负极是Al片,此时,正极的电极反应式是______________,溶液中的H+向______极移动,tl时,原电池中电子流动方向发生改变,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
下列说法中正确的是
A. 电子云通常是用小黑点来表示电子的多少
B. 处于最低能量的原子叫基态原子
C. 能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动
D. 电子仅在激发态跃迁到基态时才会产生原子光谱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com