
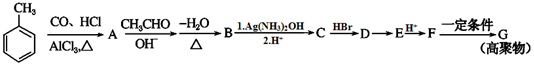
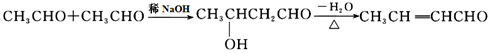
 ��
��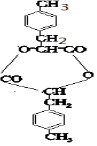 ��
�� ��
��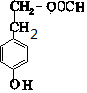 ��
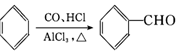
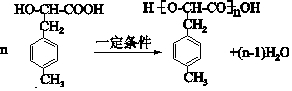
�� ���� �ױ�������Ϣ��1���еķ�Ӧ����A���һ�����A�����ϵ�һ�ȴ���ֻ�����֣���֪AΪ ��A������Ϣ��2���еķ�Ӧ����
��A������Ϣ��2���еķ�Ӧ���� ���ٷ�����ȥ��Ӧ����BΪ
���ٷ�����ȥ��Ӧ����BΪ ��B��������CΪ
��B��������CΪ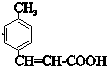 ��C��HBr�����ӳɷ�Ӧ����DΪ
��C��HBr�����ӳɷ�Ӧ����DΪ ��
�� ��
��
������F���γ���Ԫ������˵��F���Ȼ��Ħ�-̼�������ǻ�����Dֻ��Ϊ ��Dˮ������EΪ
��Dˮ������EΪ ����������FΪ
����������FΪ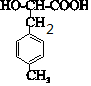 ��F�������۷�ӦGΪ
��F�������۷�ӦGΪ ���Դ������
���Դ������
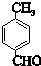
��� �⣺��1��A�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��BΪ �������ŵ�������̼̼˫����ȩ����������˳���֪����B�й����ŵ��Լ�Ϊ������Һ��������������ͭ������ˮ���ȼ���-CHO���ټ���˫����
�������ŵ�������̼̼˫����ȩ����������˳���֪����B�й����ŵ��Լ�Ϊ������Һ��������������ͭ������ˮ���ȼ���-CHO���ټ���˫����
�ʴ�Ϊ��̼̼˫����ȩ����������Һ��������������ͭ������ˮ��
��3��C��D�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��D��EΪ±������ˮ�ⷴӦ����Ӧ����ΪNaOHˮ��Һ�����ȣ�
�ʴ�Ϊ���ӳɷ�Ӧ��NaOHˮ��Һ�����ȣ�
��4��������F�γɵ���Ԫ�����Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��F��G��Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��6��FΪ ���л���H��F��һ��ͬϵ���Է���������F��14��H�г������⣬������3��C������������H��ͬ���칹��������a��������ֻ������ȡ�����Ҵ��ڶ�λ��b�����ܷ���ˮ�ⷴӦҲ����FeCl3��Һ��Ӧ����֪һ������-OH��-COOC-����-OH�뱽��ֱ������������һ��ȡ����Ϊ-CH2CH2OOCH��-CH��CH3��OOCH��-CH2OOCCH3��-OOCCH2CH3����4�֣����к˴Ź���������6���壬�����֮��Ϊ2��2��2��2��1��1�Ľṹ��ʽΪ
���л���H��F��һ��ͬϵ���Է���������F��14��H�г������⣬������3��C������������H��ͬ���칹��������a��������ֻ������ȡ�����Ҵ��ڶ�λ��b�����ܷ���ˮ�ⷴӦҲ����FeCl3��Һ��Ӧ����֪һ������-OH��-COOC-����-OH�뱽��ֱ������������һ��ȡ����Ϊ-CH2CH2OOCH��-CH��CH3��OOCH��-CH2OOCCH3��-OOCCH2CH3����4�֣����к˴Ź���������6���壬�����֮��Ϊ2��2��2��2��1��1�Ľṹ��ʽΪ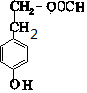 ��
��
�ʴ�Ϊ��4��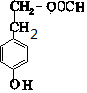 ��
��
���� ���⿼���л���ĺϳɣ�Ϊ��Ƶ���㣬����ϰ���е���Ϣ���ϳ������й����ŵı仯�������������ʡ��л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ͬ���칹����дΪ�����ѵ㣬��Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | п����ϡ���ᷴӦ��Zn+2H+=Zn2++H2�� | |
| B�� | ϡ������뵽����������Һ�У�H++OH-=H2O | |
| C�� | �Ȼ�����Һ�м��������ˮ��Al3++3NH3•H2O=Al��OH��3��+3NH4+ | |
| D�� | ����ˮ��Ӧ��Na+2H2O=Na++2 OH-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
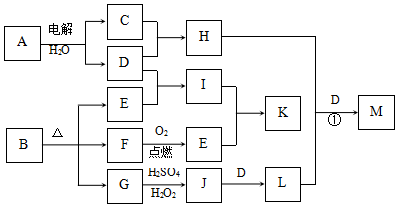
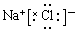 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ����ԭ�� ����ԭ�� | B�� |  ���۷��� ���۷��� | C�� |  ��ˮ���� | D�� |  ���ó��� ���ó��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 9.2g NO2��N2O4�Ļ�����к���ԭ����ĿΪ0.2NA | |
| B�� | ���³�ѹ�£�35.5g Cl2��������NaOH��Һ��ȫ��Ӧ��ת�Ƶĵ�����ΪNA | |
| C�� | ��״���£�2.24L NH3��1.6g CH4����������������Ŀ��ΪNA | |
| D�� | ��֪��ӦN2��g��+3H2��g��?2NH3��g����H=-92.4 kJ•mol-1��������NA��NH3����ʱ����Ӧ�ų�������С��46.2kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ŵ��������� | |
| B�� | ʯ������Һ����ú��Һ�� | |
| C�� | �鼮�е�ֽ���ɰ�ɫ������ɻ�ɫ | |
| D�� | ������ˮ�Ե�ֲ����ά�ĸ������ˮ�Ͱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2A��l��+B��l���T2C��g����H | B�� | 2A��g��+B��g���T2C��g����H | C�� | 2A��l��+B��l���T2C��l����H | D�� | 2A��g��+B��g���T2C��l����H |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com