
已知化学反应2C(s)+O2(g)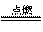 2CO(g);2CO(g) + O2(g)
2CO(g);2CO(g) + O2(g)  2CO2(g)都是放热反应。
2CO2(g)都是放热反应。 据此推断,下列说法不正确的是(相同条件下)
据此推断,下列说法不正确的是(相同条件下)
A.56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量
B.28gCO所具有的能量一定高于12gC所具有的能量
C.12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D.将两份等质量碳燃烧,生成CO2的反应比生成CO的反应放出的热量多
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
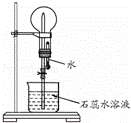
A是一种白色晶体,受热分解能生成B、C两种无色气体,C的水溶液与硝酸银溶液反应产生白色沉淀.A与浓NaOH溶液共热,放出无色气体B.若在圆底烧瓶中分别收集干燥的气体B和C,然后将收集满气体的烧瓶按如图所示装置组装,挤压滴管的胶头时,可以分别得到蓝色喷泉和红色喷泉.
请填写下列空白:
(1)A的化学式是 ;
(2)收集气体B的方法是 ;
(3)B与C两气体相遇时,可观察到的现象是 ;
(4)A与浓NaOH溶液共热时,发生反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知锰的核电荷数为25,以下是一些同学绘制的基态锰原子核外电子的轨道表示式(即电子排布图),其中最能准确表示基态锰原子核外电子运动状态的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
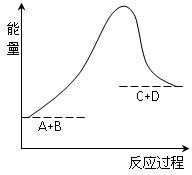
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是
A.该反应为放热反应 B.该反应为吸热反应
C.反应物的总能量高于生成物的总能量 D.该反应只有在加热条件下才能进行
查看答案和解析>>
科目:高中化学 来源: 题型:
根据盖斯定律判断右图所示的物质转变过程中,正确的是

A.ΔH1=ΔH2=ΔH3=ΔH4 B.ΔH1+ΔH2=ΔH3+ΔH4
C.ΔH1+ΔH2+ΔH3=ΔH4 D.ΔH1=ΔH2+ΔH3+ΔH4
查看答案和解析>>
科目:高中化学 来源: 题型:
炽热的炉膛内有反应:C(s)+O2(g)=CO2(g),△H=-392kJ·mol—1 往炉膛内通入水蒸汽时,有如下反应:C(s)+H2O(g)=CO(g)+H2(g),△H=+131 kJ·mol—1 CO(g) + 1/2O2(g)= CO2(g),ΔH=-282 kJ·mol—1
H2(g)+1/2O2(g)=H2O(g),△H=-241kJ·mol—1,由以上反应推断往炽热的炉膛内通入水蒸汽时( )
A、既能使炉火更旺,又能节省燃料
B、虽不能使炉火更旺,但可以节省燃料
C、不能节省燃料,但能使炉火瞬间更旺
D 、既不能使炉火更旺,又不能节省燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
工业生产水煤气的反应为:
C(s)+H2O(g) 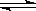 CO(g)+H2(g) ΔH =+131.4kJ·mol-1,下列判断正确的是
CO(g)+H2(g) ΔH =+131.4kJ·mol-1,下列判断正确的是
A.反应物能量总和大于生成物能量总和
B.CO(g)+H2(g) 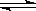 C(s)+H2O(l)ΔH =-131.4kJ·mol-1
C(s)+H2O(l)ΔH =-131.4kJ·mol-1
C.水煤气反应中生成1molH2(g)吸收131.4 kJ热量
D.水煤气反应中生成1L CO(g)吸收131.4 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
关于反应CaO + 3C→CaC2 + CO,下面哪种表述能最好地说明该反应是一个氧化还原反应
A. CaO失氧变为CaC2 B. C的状态发生了变化
C. Ca的化合价在反应前后发生了改变 D. C失去了电子,同时也得到了电子
查看答案和解析>>
科目:高中化学 来源: 题型:
碘是人体中不可缺少的微量元素。食盐中加入碘元素能有效防止缺碘引起的疾病。以前在食盐中加入碘化钾(KI),放置一年后,碘流失约92%。现在食盐中加入碘酸钾(KIO3),在相同条件下碘仅损失约7%
(1)、食盐中加入碘化钾的碘损失率高的原因是 ;
(2)、萃取碘水中的碘时,一般选用的试剂是(填字母) ;
A、酒精 B、四氯化碳 C、乙酸
(3)、可用盐酸酸化的碘化钾和淀粉溶液检验食盐中的碘酸钾。反应的化学方程式为:
5KI+KIO3 + 6HCl == 6KCl + 3I2 + 3H2O,反应的现象是 ;
(4)、已知碘酸钾受热易分解,你认为在用碘酸钾加碘盐进行烹饪时应注意什么问题?
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com