
| A. | 金属钠着火时,立即用水灭火 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中 | |
| C. | 用点燃的火柴在液化气钢瓶口检验是否漏气 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处走 |
分析 A.金属钠及其燃烧产物都能够与水反应,不能用水灭火;
B.浓硫酸密度大于水,且稀释过程中放出大量热,应该将浓硫酸倒入水中;
C.液化气容易发生爆炸,不能使用灭火检验液化气是否漏气;
D.氯气有毒,氯气的密度大于空气,低处氯气的含量大.
解答 解:A.钠、过氧化钠都能够与水反应,用水无法灭火,可以使用沙子灭火,故A错误;
B.稀释浓硫酸时,由于稀释过程放出大量的热,且浓硫酸密度大于水的密度,所以应该将浓硫酸缓缓加入水中,顺序不能颠倒,故B错误;
C.液化气遇到灭火容易发生爆炸,所以不能用点燃的火柴在液化气钢瓶口检验是否漏气,可以使用肥皂水检验,故C错误;
D.氯气密度大于空气,低处氯气含量较大,所以大量氯气泄漏时,迅速离开现场并尽量往高处去,故D正确;
故选D.
点评 本题考查了化学安全事故及处理方法,题目难度中等,注意掌握常见化学试剂的性质及安全事故处理方法,遇到突发事故时一定要冷静处理,保证人身和国家财产安全.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 分别表示N2、H2、NH3):
分别表示N2、H2、NH3):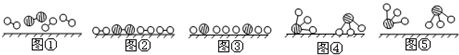
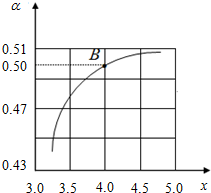 的量之比(氨碳比)$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=x,如图是CO2平衡转化率(α) 与氨碳比(x)的关系.
的量之比(氨碳比)$\frac{n(N{H}_{3})}{n(C{O}_{2})}$=x,如图是CO2平衡转化率(α) 与氨碳比(x)的关系.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

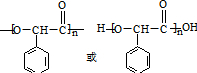
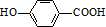 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤④①③② | B. | ⑤③④②① | C. | ②④③①⑤ | D. | ③②④⑤① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol?L-1K2SO4含有的K+数目为NA | |
| B. | 56g铁与足量的盐酸反应时失去电子的数目为3NA | |
| C. | 在标准状况下,22.4LCCl4中含有的分子数目为NA | |
| D. | 在常温常压下,16gO2和O3的混合气体所含原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
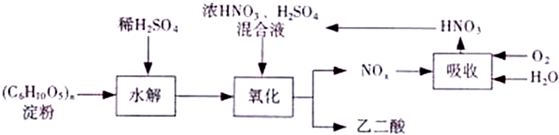
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸、亚硫酸和次氯酸都是见光易分解的挥发性酸 | |
| B. | 合金属于金属单质,很多性能与组成它的纯金属不同 | |
| C. | 金属及其氧化物、氢氧化物都不可能与强碱溶液反应 | |
| D. | 元素的非金属性、金属性强弱与其得失电子数目无直接关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com