
| A. | 体积大小:③>②>① | B. | 原子数目:③>①>② | C. | 密度大小:②>③>① | D. | 质量大小:②>①>③ |
分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$分别计算出三种物质的量的物质的量,
A.相同条件下气体体积之比等于其物质的量之比;
B.根据各物质的分子组成及物质的量计算出含有原子数目;
C.由ρ=$\frac{M}{{V}_{m}}$可知,相同条件下密度之比等于摩尔质量之比;
D.根据m=nM计算出各物质的质量大小.
解答 解:①6.72L NH3的物质的量为:$\frac{6.72L}{22.4L/mol}$=0.3mol;
②1.204×1023个 H2S 的物质的量为:$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.2mol;
③5.6g CH4的物质的量为:$\frac{5.6g}{16g/mol}$=0.35mol,
A.根据V=nVm知,相同条件下体积之比等于物质的量之比,故体积③>①>②,故A错误;
B.原子的物质的量分别为0.3mol×4、0.2mol×3、0.35mol×5,则原子数目:③>①>②,故B正确;
C.由ρ=$\frac{M}{{V}_{m}}$可知,相同条件下,密度之比等于摩尔质量之比,故密度②>①>③,故C错误;
D.根据m=nM知,氨气的质量为0.3mol×17g/mol=5.1g,H2S的质量为0.2mol×34g/mol=3.8g,则质量大小:②>③>①,故D错误;
故选B.
点评 本题考查了阿伏伽德罗定律及其推论,明确物质的量的基本公式中各个物理量之间的关系是解本题关键,灵活运用基本公式分析解答即可,题目难度中等.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物水化物的碱性:Y<Z | B. | 简单气态氢化物的热稳定性:X<W | ||
| C. | 简单气态氢化物的沸点:X<W | D. | 简单离子的还原性:X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
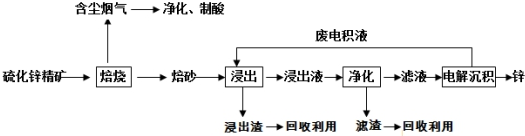
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
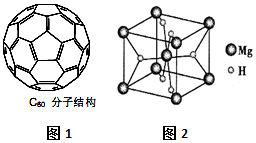 氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等.
氢的存储是氢能应用的主要瓶颈,目前所采用或正在研究的主要储氢材料有:配位氢化物、富氢载体化合物、碳质材料、金属氢化物等. D.相同压强时,NH3沸点比PH3高
D.相同压强时,NH3沸点比PH3高查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 化学变化中一定发生物理变化 | |
| B. | 蓄电池充电时,电能转变成化学能 | |
| C. | 人类利用的能量都是通过化学反应获得的 | |
| D. | 有颜色改变的变化一定是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NO2(g)?N2O4(g) | B. | 2HI(g)?H2(g)+I2(g) | ||
| C. | PCl5?PCl3(g)+Cl2(g) | D. | CaCO3(s)?CaO(g)+CO2 (g) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①④⑤ | D. | ①③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com