
【题目】用中和滴定法测定某盐酸的物质的量浓度。
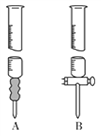
(1)标准溶液应盛于___________(填“A”或“B”)滴定管中。
(2)若选用酚酞作指示剂,以0.1250 mol·L-1的标准氢氧化钠溶液滴定,如何判断滴定终点____________。
(3)实验数据记录如下表,请分析数据并计算,盐酸的物质的量浓度=_________mol·L-1。
滴定次数 | 待测溶液体积/mL | ||
标准碱液 | |||
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.00 | 16.02 |
2 | 20.00 | 0.00 | 15.98 |
3 | 20.00 | 0.00 | 16.00 |
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是( )
A.Fe3+、NH4+、SCN﹣、Cl﹣
B.Na+、H+、NO3﹣、SO42﹣
C.Fe2+、Fe3+、Na+、NO3﹣
D.Fe2+、NH4+、Cl﹣、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是
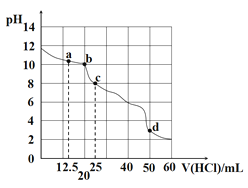
A.a点:c(A2-)=c(HA-)
B.b点:5c(Cl-)=4[c(A2-)+c(HA-)+c(H2A)]
C.c点:c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.d点:c(H+)=c(HA-)+c(A2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,下列各组离子在指定溶液中能大量共存的是
A.c(Fe3+)=0.1 mol/L溶液中:Na+、NH![]() 、SCN-、SO
、SCN-、SO![]()
B.能溶解CaCO3的溶液中:Fe3+、Ca2+、Cl-、NO![]()
C.由水电离出的c(H+)=1×10-2mol/L的溶液中:Na+、Ba2+、HCO![]() 、Cl-
、Cl-
D.强碱性溶液中:K+、Na+、ClO-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属的使用是人类拓展自身能力的标志之一。人类利用几种常用金属的先后顺序依次为金、铜、铁、铝,之所以有先后,主要取决于( )
A. 金属在地壳中的含量多少 B. 金属的熔沸点高低
C. 金属的活泼性强弱 D. 金属的导电性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol乙醇(其中的羟基氧用18O标记)在浓硫酸存在下并加热与足量乙酸充分反应。下列叙述不正确的是( )
A. 生成的乙酸乙酯中含有18O B. 生成的水分子中含有18O
C. 可能生成45g乙酸乙酯 D. 不可能生成90g乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+ O2![]() 2MnO2+2CO2。经研究发现该反应过程为①MnCO3
2MnO2+2CO2。经研究发现该反应过程为①MnCO3![]() MnO+ CO2;②2MnO +O2
MnO+ CO2;②2MnO +O2![]() 2MnO2。
2MnO2。
回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2,用平衡分压代替平衡浓度,碳酸锰热分解反应的平衡常数K=________(分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2的关系为_________________。
(2)反应②在低温下能自发进行,则其△H__________0 (填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com